
【题目】根据问题填空:
(1)下列原子: ![]() C、147N、
C、147N、 ![]() Na、
Na、 ![]() H、
H、 ![]() U、
U、 ![]() K、
K、 ![]() U中共有种元素,种核素,和互为同位素.
U中共有种元素,种核素,和互为同位素.
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(X为核电荷数,Y为元素的 有关性质).把与下面元素有关的性质相符的曲线标号填入相应的空格中: 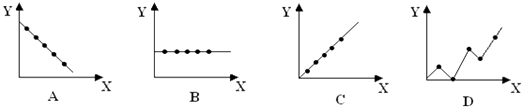
② 第ⅡA族元素的最外层电子数;
②第三周期元素的最高化合价;
③碱金属单质的熔点
(3)阴离子的中子数为N:AXn﹣共有x个电子,则N= .
(4)有下列物质中NH3、Na2O、CO2、CaCl2、CCl4、N2、NaHCO3、NaOH、Na2O2、NH4Cl属于电解质的有 .
【答案】
(1)6;7; ![]() U;
U; ![]() U
U
(2)B;C;A
(3)A﹣x+n
(4)6个
【解析】解:(1)原子:: ![]() C、147N、
C、147N、 ![]() Na、
Na、 ![]() H、
H、 ![]() U、
U、 ![]() K、
K、 ![]() U质子数都92,属于同一元素,所以共有6种元素,具有一定数目质子和一定数目中子的一种原子叫做核素,所以共有7种核素,原子AZX,中子数(N)=质量数(Z)﹣质子数(A),
U质子数都92,属于同一元素,所以共有6种元素,具有一定数目质子和一定数目中子的一种原子叫做核素,所以共有7种核素,原子AZX,中子数(N)=质量数(Z)﹣质子数(A), ![]() U、
U、 ![]() U质子数都92,中子数不同,属于同位素,
U质子数都92,中子数不同,属于同位素,
所以答案是:6、7、 ![]() U、
U、 ![]() U;(1)6、7、
U;(1)6、7、 ![]() U、
U、 ![]() U(2)①ⅡA族元素的最外层电子数相等,图象B符合,所以答案是:B;②第3周期的最高化合价从左→右依次升高,图象C符合,所以答案是:C;③因碱金属属于金属晶体,半径越大,金属键越弱,熔沸点越低,则碱金属单质的熔点随原子序数的增大而降低,图象A符合,所以答案是:A.(2)、①B、②C、③A (3)阴离子的中子数为N:AXn﹣共有x个电子,所以质子数为:x﹣n,根据中子数(N)=质量数(Z)﹣质子数(A)=A﹣x+n,所以答案是:A﹣x+n;(4)NH3是非电解质;Na2O是电解质;CO2是非电解质;CaCl2是电解质;CCl4是非电解质;N2是单质;NaHCO3是电解质;NaOH是电解质;Na2O2是电解质;NH4Cl是电解质;所以属于电解质的有6个,所以答案是:6个.
U(2)①ⅡA族元素的最外层电子数相等,图象B符合,所以答案是:B;②第3周期的最高化合价从左→右依次升高,图象C符合,所以答案是:C;③因碱金属属于金属晶体,半径越大,金属键越弱,熔沸点越低,则碱金属单质的熔点随原子序数的增大而降低,图象A符合,所以答案是:A.(2)、①B、②C、③A (3)阴离子的中子数为N:AXn﹣共有x个电子,所以质子数为:x﹣n,根据中子数(N)=质量数(Z)﹣质子数(A)=A﹣x+n,所以答案是:A﹣x+n;(4)NH3是非电解质;Na2O是电解质;CO2是非电解质;CaCl2是电解质;CCl4是非电解质;N2是单质;NaHCO3是电解质;NaOH是电解质;Na2O2是电解质;NH4Cl是电解质;所以属于电解质的有6个,所以答案是:6个.


科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“ ![]() ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的TS核素符号是 ![]() Ts
Ts
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取三张湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加98.3%的硫酸、新制氯水、浓氨水,三张试纸最后呈现的颜色是
A.红、白、蓝B.黑、白、蓝C.白、白、蓝D.黑、红、蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2A(g)2B(g)+E(g)-Q,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
A.加压B.减压C.增加E的浓度D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质按要求填空 ①131I 与132I ②C60与石墨 ③CH3Cl 与CH3CH2Cl ④硫酸氢钠 ⑤氯化镁 ⑥氩
⑦过氧化氢 ⑧ ![]() 与
与 ![]() ⑨CS2
⑨CS2
⑩过氧化钠
(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同系物的是
(4)⑧中两种物质的关系是(同系物,同素异形体,同一种物质)
(5)含共价键的离子化合物
(6)仅含共价键的物质
(7)用电子式表示⑨的形成过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一个V升固定容积的密闭容器中,发生如下反应:N2 (g)+3H2(g)═2NH3(g)
(1)若反应进行到t分钟时,nt(N2)=13mol,nt(NH3)=6mol,计算a= , 反应速率V(H2)=molL﹣1min﹣1 .
(2)下列描述中能表明反应已达到平衡状态的是 ①混合气体的压强不变 ②混合气体的密度不变 ③混合气体的平均摩尔质量不变
④容器内N2 , H2 , NH3的浓度之比为1:3:2 ⑤单位时间内生成n mol NH3 , 同时生成N2 , H2共2n mol
(3)反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%.计算平衡时NH3的物质的量n(NH3)=mol,N2和H2的转化率之比,α(N2):α(H2)= . (写最简整数比)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两种烃,A常用作橡胶、涂料、清漆的溶剂,胶粘剂的稀释剂、油脂萃取剂。取0.1molA在足量的氧气中完全燃烧,生成13.44LCO2气体(标准状况下测定),生成的H2O与CO2的物质的量之比为1:1。则:
(1)A的分子式为___________________________。
(2)A的同分异构体较多。其中:①主链有五个碳原子;②能使溴的四氯化碳溶液和高锰酸钾酸性溶液褪色;③在Ni催化下能与氢气发生加成反应。符合上述条件的同分异构体有:![]() 、
、
![]() 、
、![]() 、
、![]() 、___________________、_____________________ (写结构简式,不考虑顺反异构)。
、___________________、_____________________ (写结构简式,不考虑顺反异构)。
写出用![]() 在一定条件下制备高聚物的反应方程式_____________________,反应类型为____________________。
在一定条件下制备高聚物的反应方程式_____________________,反应类型为____________________。
(3)B与A分子中磯原子数相同,1866年凯库勒提出B分子为单、双键交替的平面结构,解释了B的部分性质,但还有一些问题尚未解决,它不能解释下列事实中的______________。
a.B不能使溴水褪色 b.B能与发生加成反应
c.B的一溴代物没有同分异构体 d.B的邻位二溴代物只有一种
(4)M是B的同系物,0.1molM在足量的氧气中完全燃烧,产生标准状况下15.68L二氧化碳。
①写出下列反应的化学方程式:
M光照条件下与Cl2反应:______________________________。
M与浓硝酸和浓硫酸的混合酸加热:_____________________________________。
②M________(填“能”或“不能”)使高锰酸钾酸性溶液褪色,M与氢气加成产物的一氯代物有____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2 . 在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
A.Cu与Cu2O的物质的量之比为2:1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO在标准状况下的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com