
| A. | 0.448L | B. | 0.336L | C. | 0.224L | D. | 无法计算 |
分析 铜与稀硝酸反应的实质是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,只要Cu与硫酸足量,NO3-可以被完全还原,n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,计算溶液中H+、NO3-的物质的量,根据离子方程式进行过量计算,根据不足量的物质计算n(NO),再根据V=nVm计算NO体积.
解答 解:n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,
n(H+)=2×0.01mol+0.04mol=0.06mol,n(NO3-)=0.04mol,
3 Cu+2 NO3-+8 H+=3Cu2++2NO↑+4H2O
0.03mol 0.02mol 0.08mol
则H+不足,Cu、NO3-过量,由方程式可知n(NO)=$\frac{1}{4}$×0.06mol=0.015mol,
所得NO体积在标准状况下为0.015mol×22.4L/mol=0.336L,
故选B.
点评 本题考查化学方程式有关计算,题目难度中等,注意酸性条件下硝酸根有强氧化性,利用离子方程式进行过量计算,避免利用化学方程式的繁琐计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 2:3 | C. | 7:6 | D. | 7:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱:HClO4>H2SO4>H3PO4 | B. | 离子半径:Na+>Mg2+>Al3+>F- | ||
| C. | 热稳定性:HCl>H2S>PH3>SiH4 | D. | 氧化性:K+<Na+<Mg2+<Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④<①<③<② | B. | ①<④<③<② | C. | ①<②<③<④ | D. | ④<③<①<② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
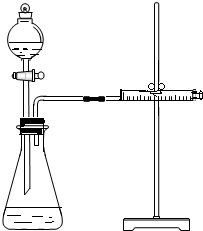 影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:
影响化学反应速率的因素很多,某学校化学小组用实验的方法进行探究.他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来探究影响化学反应速率的因素.甲同学的实验报告如下表:| 实验步骤 | 现象 | 结论 |
| ①分别取等体积2mol/L的硫酸于试管中 ②分别投入大小、形状相同的Cu、Fe、Mg | 反应速率Mg>Fe,Cu反应最慢 | 金属性质越活泼,反应 速率越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 125g CuSO4•5H2O晶体中含有Cu2+离子数一定小于0.5NA | |
| B. | 常温下,pH=3的醋酸溶液中,醋酸分子的数目一定大于10-3NA | |
| C. | 由S6、S7、S8组成的硫蒸气6.4g,其中所含硫原子数一定为0.2NA | |
| D. | 3.6g C与3.36L O2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式为: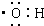 | |
| B. | 甘氨酸的结构简式为:C2H5NO2 | |
| C. | 间羟基苯甲酸的结构简式为: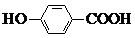 | |
| D. | Na2S在溶液中水解的离子方程式为:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能描述出反应发生的状态 | B. | 说明反应条件 | ||
| C. | 为了区别一般的化学方程式 | D. | 物质呈现的状态与反应热有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com