
【题目】某化合物由两种单质直接反应生成,将其加入BaHCO3溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A.AlCl3 B.Na2O C.FeCl2 D.SiO2
 培优口算题卡系列答案
培优口算题卡系列答案科目:高中化学 来源: 题型:
【题目】2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德·埃特尔。他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是
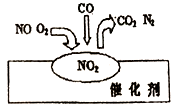
A.NO2是该过程的最终产物
B.NO 和O2必须在催化剂表面才能反应
C.汽车尾气的主要污染成分是CO2和NO
D.该催化转化的总反应方程式为:2NO+O2+4CO![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Cl2性质的说法不正确的是
A. 是无色无味的气体
B. 不能使干燥的有色布条褪色
C. 与石灰乳反应可制得漂白粉
D. 每个分子中有1个共用电子对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C的第一电离能由大到小的顺序为_______________(用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是________(填化学式),该分子中心原子的杂化轨道类型为_____________。
(3)A、C分别形成的常见的含氧酸分子中,中心原子的价层电子对数为4的酸是______(填化学式,下同),酸根呈平面三角形的酸是________________。
(4)Dn+、Br-、C的最高价含氧酸跟、A的简单氢化物按1:1:1:5形成某配合物,向该配合物的溶液中滴加AgNO3溶液产生淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物中的配体为___________,n值为__________,Dn+的基态电子排布式为____________。
(5)立方EB晶体的结构如图所示,其晶胞边长为apm,列式表示EB晶体的密度为__________g·cm-3(不必计算出结果,阿伏伽德罗常数的值为NA)。人工制备的EB晶体中常存在缺陷:一个E2+空缺,另有两个E2+被两个E3+所取代,其结果晶体仍呈电中性,但化合物中E和B的比值却发生了变化。已知某化合物样品组成E0.96B,该晶体中E3+与E2+的离子个数之比为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g)![]() 2C(g)达到平衡的标志的是( )
2C(g)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等;
②单位时间内有amolA生成的同时生成3amolB;
③A、B、C的浓度不再变化;
④容积不变的密闭容器中混合气体的总压强不再变化;
⑤混合气体的物质的量不再变化;
⑥单位时间消耗amolA,同时生成3amolB ;
⑦A、B、C的分子数目之比为1:3:2。
A.②⑤ B.②⑦ C.①③ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子:
(1)I-、Fe2+、NO3-、H+
(2)K+、NH4+、HCO3-、OH-
(3) MnO4-、H+、K+、Cl-
(4)Fe2+、Cu2+、SO42-、Cl-
(5) Na+、K+、Al3+、HCO3-
(6) 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I-
(7)室温下 ![]() 溶液中:Fe2+、NH4+、SO32-、Cl-
溶液中:Fe2+、NH4+、SO32-、Cl-
(8) 0.2 mol/L的NaNO3溶液:H+、Fe2+、SO42-、Cl-
在澄清透明溶液中能大量共存的组别共有
A.1组 B.2组 C.3组 D.不少于4组
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料。Z的非金属性在同周期元素中最强。下列说法正确的是

A. 对应简单离子半径:X>W
B. 对应气态氢化物的稳定性:Y>Z
C. 化合物XZW既含离子键,又含共价键,属于弱电解质
D. Y的氧化物和Z的氢化物均能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,正确的是( )
A. 酸性:H2SO4﹤HClO B. 气态氢化物稳定性:HCl>H2S
C. 离子半径:Na+>F- D. 碱性:NaOH>KOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com