
| A. | SO2+H2O═H2SO3 | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | 2SO2+O2$\frac{\underline{\;V_{2}O_{5}\;}}{△}$2SO3 | D. | SO2+2H2S═3S↓+2H2O |
科目:高中化学 来源: 题型:多选题
| A. | 3 v (N2)=v(H2) | B. | v (N2)=3v(H2) | C. | 1.5v (H2)=v(NH3) | D. | v (N2)=2v(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
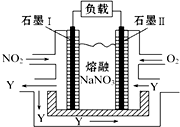 NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.
NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | CH3CH2CH2CH3和CH3CHCH3CH3 | ||
| C. | 红磷和白磷 | D. | 甲烷和乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
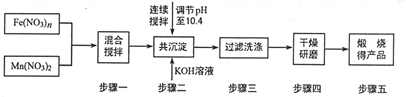 随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:(提示:锰元素在本题所有过程中价态均不变).
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:(提示:锰元素在本题所有过程中价态均不变).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com