
 X2����������в���ȱ�ٵ����壬Y�ǵؿ��к������Ľ���Ԫ�أ�ZԪ�ص���ɫΪ��ɫ��W2��һ�ֻ���ɫ���壮��ش��������⣺
X2����������в���ȱ�ٵ����壬Y�ǵؿ��к������Ľ���Ԫ�أ�ZԪ�ص���ɫΪ��ɫ��W2��һ�ֻ���ɫ���壮��ش��������⣺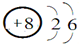 ���ʴ�Ϊ��Na��
���ʴ�Ϊ��Na��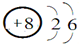 ��
��
| ||


 ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� | ʵ��Ŀ�� | |
| A | ��SO2ͨ��Ʒ����Һ�� | ֤��SO2����Ư���� |
| B | ��pH��ֽ�ⶨNaHSO3��Һ��pH | �Ƚ�HSO3-����̶Ⱥ�ˮ��̶ȵĴ�С |
| C | ��������NaOH�Ҵ���Һ���ȣ����õ�������ͨ��KMnO4������Һ | ֤����Ӧ�õ�����������ϩ |
| D | ��̪��Na2CO3��Һ�м���BaC12��Һ | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuCl2[CuSO4] |
| B��NaOH[H2O] |
| C��NaCl[H2O] |
| D��CuSO4[Cu��OH��2] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCO3-+H2O?H3O++CO32- |
| B��Fe3++3H2O?Fe��OH��3+3H+ |
| C��HS-+H2O?H2S+OH- |
| D��HCOOH+H2O?HCOO-+H3O+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ļ�ѧ���ʲ����ã��ڳ����²���������Ӧ |
| B��SiO2��CO2�������������������ǿ����Һ��Ӧ |
| C��SiO2��CO2 ��������ˮ����ˮ��Ӧ������Ӧ���� |
| D�������ڷǽ����������õİ뵼����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������֪Ũ�ȵ�����ζ�δ֪Ũ�ȵ�����������Һ�յ�ʱ���Ӷ�������������Ũ��ƫ�� |
| B��pH=13����Һ�У�CO32-��Na+��AlO2-��NO3- �ܴ������� |
| C����500mL 1 mol/L Na2CO3��Һ�У��μ�600mL 1 mol/L HCl�õ������CO2���Ϊ11.2L |
| D���ö��������ɼ�������Һ��������Һ����������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������NaCl��Һ |
| B��ϡNaHSO4��Һ |
| C��MgCl2��Һ |
| D��CuSO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2��g��������������HI��g������������֮��Ϊ2��1 |
| B�������淴Ӧ���ʵı�ֵ�Ǻ㶨�� |
| C����HI�ķ�������I2������֮��Ϊ2��1ʱ��˵����Ӧ�ﵽ��ƽ��״̬ |
| D���ﵽƽ��ʱ�������淴Ӧ������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com