
| 酸 | HX | HY | HZ | ||||||||||||||||||
| 浓度mol/L | 0,1 | 0.5 | 0.9 | 1 | 1 | ||||||||||||||||
| 电离度% | 0.3 | 0.15 | 0.1 | 0.3 | 10
练习册系列答案
 一线名师提优试卷系列答案 一线名师提优试卷系列答案
相关习题
科目:高中化学 来源:不详 题型:单选题 下列关于电解质溶液的判断正确的是
查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 ①25℃,难溶电解质的溶度积常数:Ksp[CaF2]=1.5×10-10,Ksp[Mg(OH)2]=1.8×10-11,Ksp [Cu(OH)2]=2.2×10-20 ②弱电解质在水溶液中存在电离常数:例如一元弱酸HA 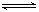 H++A-,其电离常数表达式 Ka= c(H+)·c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5 H++A-,其电离常数表达式 Ka= c(H+)·c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5③25℃时,2.0×10-3mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到 c(HF)、c(F-)与溶液pH的变化关系,如下图所示: 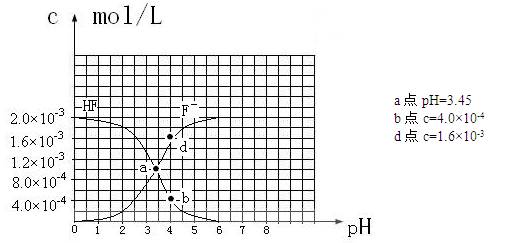 请根据以上信息回答下列问题: (1)25℃时,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。 (2)25℃时,HF电离常数的数值Ka 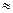 ,列式并说明得出该常数的理由 。 ,列式并说明得出该常数的理由 。(3)25℃时,向浓度均为0.1 mol·L-1的相同体积的HF和醋酸两种溶液中分别加入相同的足量锌粒,初始时产生氢气的速率关系为 (填“>”“=”或“<”,下同)。反应结束后,产生氢气的物质的量的关系为 ,两溶液中c (F-) c (CH3COO-)。 (4)25℃时,4.0×10-3mol·L-1HF溶液与4.0×10-4 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 【3分】下列各项操作,能发生“先沉淀后溶解”现象的是( )
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 (1)(3分)在无土栽培中,配制1 L内含0.5 mol NH4Cl、0.16 mol KCl、0.24 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为: 、_________ 、_______。 (2)(4分)下列物质:①烧碱 ②液态HCl ③SO3 ④铁片 ⑤石墨 ⑥CO2 ⑦醋酸 ⑧碳酸钙中, 属于电解质的是  (填编号,下同), (填编号,下同),属于非电解质的是 。 查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 请将正确的序号填入空白处。下列物质中 ⑴属于电解质的是 ⑵属于非电解质的是 ⑶属于单质的是 ① 空气 ②铜 ③硫酸钡④石墨 ⑤乙醇 ⑥SO2 ⑦H2SO4⑧CaO⑨盐酸 ⑩熔融的NaOH 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 有关电解质的说法正确的是
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 | ||||||||||||||||