
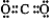 ���ʴ�Ϊ��C2H4O��
���ʴ�Ϊ��C2H4O��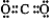 ��
��
| ||
| ||
| 0.6mol |
| 0.3L |
| 1.2mol |
| 0.3L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£����������Һ�еμ���������Һ������һ���У�c��CH3COOH��=c��Cl-�� |
| B��ij��ʽ��NaHA��Һ��һ���У�c��OH-��+c��A2-��=c��H+��+c��H2A�� |
| C��������pHΪ2�����ᣬH2O�������c��H+��=1.0��10-2mol?L-1 |
| D�������£���50mL 0.1mol?L-1��������100mL 0.1 mol?L-1�İ�ˮ��ϣ�������Һ�У�c��NH3?H2O����c��Cl-����c��NH4+����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 1mol N2��3mol H2 | 2mol N2��6mol H2 | 2mol NH3 |
| NH3��Ũ�ȣ�mol?L-1�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�Q1kJ | �ų�Q2kJ | ����Q3kJ |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 |
| A��2p1=2p3��p2 |
| B���ﵽƽ��ʱ��������NH3������������ |
| C����2+��3��1 |
| D��Q3+Q1=92.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʱ�䣨h�� ��Ԫ�� �¶� �۳��� |
1.5 | 2.5 | 3.0 | 3.5 | 4.0 |
| 830�� | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
| 890�� | 0.579 | 0.691 | 0.694 | 0.699 | 0.699 |
| 950�� | 0.669 | 0.714 | 0.714 | 0.714 | 0.714 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �״�����Ϊȼ�ϵ�ص�ԭ�ϣ���CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ���Ʊ��״���
�״�����Ϊȼ�ϵ�ص�ԭ�ϣ���CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ���Ʊ��״����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��pH=1����Һ�У�Na+��Fe2+��NO3-��SO42- |
| B��c��OH-��=10-12����Һ�У�NH4+��Al3+��NO3-��Cl- |
| C����ˮ�����c��H+��=1��10-13mol?L-1����Һ�У�Ba2+��K+��Cl-��[Al��OH��4]- |
| D����ʹ���۵⻯����ֽ����ɫ����Һ��K+��SO42-��S2-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Μ[ʯ��ˮ��ͨ�˹�����CO2��OH-+CO2=HCO3- |
| B���ں����ҵĽ���Һ������I���еμ�H2O2�õ�I2��2I-+H2O2+2H+�TI2+O2��+2H2O |
| C���Ȼ�����Һ�м��������ˮ��Al3++4NH3?H2O�TA1O2-+4NH4++2H2O |
| D��������������������������Һ��Ӧ��pHǡ��Ϊ7��H++SO42++Ba2++OH-�TBaSO4��+H2O |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com