
��1��Ԫ��M�Ƕ�����Ԫ�أ��䳣�������ں�ˮ�У����ʱ���Ϊ��������������
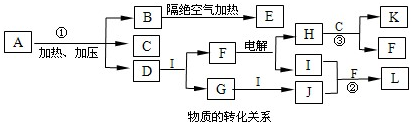
��M��ԭ�ӽṹʾ��ͼΪ______��
����M��AlΪ�缫��KOH��ҺΪ�������Һ�����ĵ缫��ӦʽΪ______��
��2������ǽ������������ȵ�ij�¶ȣ��漴�����������п�����ȴ�Ľ����ȴ������ա�
��ʹ��ˮ���д�������ɴ������������÷�Ӧ�Ļ�ѧ����ʽΪ____________
����֤����ˮ����Ĺ�������Ƿ����+3�۵�������ѡ�õ��Լ�Ϊ_______ (�����)
A��H2O2��Һ B��ͭ�� C��ϡ���� D��KMnO4��Һ
��3���{�������ˮ�еķ�ӦΪ4FeO42��+10H2O 4Fe(OH)3+8OH��+3O2
4Fe(OH)3+8OH��+3O2
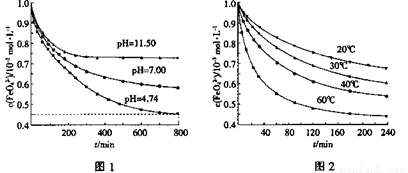
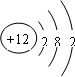
��ͼ1��25��ʱK2FeO4�ڲ�ͬpH��Һ��Ũ�ȵı仯�����pH =4.74ʱ����Ӧ�ӿ�ʼ��800min��ƽ����Ӧ����v(FeO42��)=______ (������λ��Ч���֣���
��ͼ1��800min��������Һ��K2FeO4��Ũ�Ⱦ����ٸı䡣�۲�ͼ1�ж�����pH ��˷�Ӧ��ƽ�ⳣ��______����������С�����䡱����
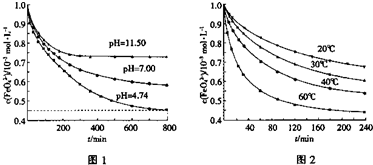
��ͼ2��240min��������Һ��K2FeO4��Ũ�Ⱦ����ٸı䣬��������Ӧ�ķ�Ӧ�� ��H______0(�>������<������=������
��15�֣���1����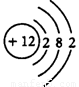 ��2�֣�
��2�֣�
��Al+4OH����3e��=[Al(OH)4]����AlO2��+2H2O��2�֣�
��2����3Fe+4H2O Fe3O4+4H2����3�֣�
Fe3O4+4H2����3�֣�
��BC��2�֣�
��3����6.9��10��7mol•L��1•mol��1��2�֣�
�ڲ��䣨2�֣�
��>��2�֣�
��������
�����������1���ٸ��������֪MΪþ���˵����Ϊ+12��������Ӳ�ṹΪ282����þ������KOH��Һ����������KOH��Һ������������������������Ӧ����ӦʽΪAl+4OH����3e��=[Al(OH)4]����AlO2��+2H2O����2���ٺ��ȵ�������ˮ��Ӧ��������������������������3Fe+4H2O Fe3O4+4H2������Fe3O4�Ǽ��������������ϡ���ᣬ����ˮ��Fe3+��Fe2+��˫��ˮ������ؾ�������Fe2+��ͭ���ܻ�ԭFe3+��Fe3+������ͭ����BC��ȷ����3���ٶ�ͼ��֪����c(FeO42��)=(1.0��0.45)��10��3mol/L���ɡ�c/��t��֪��v(FeO42��)=(1.0��0.45)��10��3mol/L��800min=6.867��10��7mol/(L•min)��6.9��10��7mol/(L•min)��������pH����¶Ȳ��䣬��ƽ�ⳣ�����䣻�������¶����ߣ�c(FeO42��)��С����ƽ�����ƣ�˵������Ӧ�����ȷ�Ӧ�����H>0��
Fe3O4+4H2������Fe3O4�Ǽ��������������ϡ���ᣬ����ˮ��Fe3+��Fe2+��˫��ˮ������ؾ�������Fe2+��ͭ���ܻ�ԭFe3+��Fe3+������ͭ����BC��ȷ����3���ٶ�ͼ��֪����c(FeO42��)=(1.0��0.45)��10��3mol/L���ɡ�c/��t��֪��v(FeO42��)=(1.0��0.45)��10��3mol/L��800min=6.867��10��7mol/(L•min)��6.9��10��7mol/(L•min)��������pH����¶Ȳ��䣬��ƽ�ⳣ�����䣻�������¶����ߣ�c(FeO42��)��С����ƽ�����ƣ�˵������Ӧ�����ȷ�Ӧ�����H>0��
���㣺����þ�Ĵ��ڡ�ԭ�ӽṹʾ��ͼ�����͵�صĸ�����Ӧʽ��������Ҫ���ʡ������仯��������ʡ���ѧ��Ӧ���ʡ���ѧƽ�ⳣ������Ӧ�ȡ��¶ȶԻ�ѧƽ���Ӱ������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����


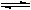 NH4++NH2-
NH4++NH2- NH4++NH2-
NH4++NH2-�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
2- 4 |
2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C��D��E��F����Ԫ�ؾ��Ƕ�����Ԫ�أ���ԭ��������������B��Fԭ�ӵ�������������Ϊ����Ӳ�����������D��FԪ��ԭ�ӵ�������������ȡ�X��Y��Z��W���ס����������ʾ�������Ԫ�ص����ֻ�����Ԫ����ɣ�Ԫ��B�γɵĵ���M��ס��Ҿ��ܷ�Ӧ����Է���������<�ң�ת����ϵ��ͼ����Ӧ������ȥ����Ԫ��E�γɵĵ����� ��21���͵���Դ������ĿǰӦ�����İ뵼����ϡ���ش��������⣺
��1��д��M���Ũ��Һ����ʱ��Ӧ�Ļ�ѧ����ʽ ��
��2��X��Y��Z��W����ͬһ�����ʣ���������̬ʱ�ľ�������Ϊ ��X��Y��W������Z��Ӧ����Z�ĽṹʽΪ ��
��3����X��W��D2��1��1��n�����ʵ���֮��ͨ��Z�У���ַ�Ӧ��������ʣ������ɣ���n= ��д����Ӧ�Ļ�ѧ����ʽ ��
��4��������ED2��Ԫ��B�γɵ�ij�ֵ��ʾ���������ͬ�����ڸ������ܷ����û���Ӧ������Ӧ��B�ĵ��ʱ��ƻ�1 mol���ۼ�����μӷ�Ӧ�Ļ�����ED2������Ϊ g��
��5��Ԫ��B����һ�ֵ��ʾ���ƽ���״�ṹ��ͬһ���е�ԭ�ӹ������������������Σ���12 g�þ����к��� NA���������Ρ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com