
等物质的量的NaHCO3和KHCO3的混合物9.20 g与100 mL盐酸反应。
(1)试分析,欲求标准状况下生成的CO2的体积时,还需什么数据(用a、b等表示,要注明单位)。
(2)求标准状况下生成的CO2的体积。
| 所需数据的取值范围 | 生成CO2的体积(标准状况) |
| 盐酸不足时 | |
| 盐酸恰好反应时 | |
| 盐酸过量时 |
(3)若NaHCO3和KHCO3不是等物质的量混合,则9.20 g固体与盐酸完全反应时,在标准状况下生成CO2气体的体积范围___________________________。
(1)a mol·L-1 (2)2.24a L 2.24 L 2.24 L (3)2.06 L<V(CO2)<2.45 L
(1)由H++![]() ====H2O+CO2↑可知,欲求标准状况下的CO2气体的体积,需确定
====H2O+CO2↑可知,欲求标准状况下的CO2气体的体积,需确定![]() 与H+过量与否,显然缺少的数据为盐酸的物质的量浓度,设为a mol·L-1。
与H+过量与否,显然缺少的数据为盐酸的物质的量浓度,设为a mol·L-1。
(2)当H+与![]() 恰好完全反应时:
恰好完全反应时:
0.1 L ·a mol·L-1=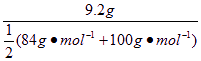 a=1 mol·L-1;若盐酸不足,则a<1 mol·L-1,产生的CO2的体积按HCl的物质的量计算:V(CO2)=2.24a L;若盐酸过量,则a>1 mol·L-1产生的CO2的物质的量等于混合物的物质的量,V(CO2)=2.24 L。
a=1 mol·L-1;若盐酸不足,则a<1 mol·L-1,产生的CO2的体积按HCl的物质的量计算:V(CO2)=2.24a L;若盐酸过量,则a>1 mol·L-1产生的CO2的物质的量等于混合物的物质的量,V(CO2)=2.24 L。
(3)盐酸足量,混合物完全反应。若9.2 g全部为NaHCO3,则产生的CO2体积:V(CO2)=![]() ×22.4 L·mol-1=2.45 L;若9.2 g全部为KHCO3,则产生的CO2体积:V(CO2)=
×22.4 L·mol-1=2.45 L;若9.2 g全部为KHCO3,则产生的CO2体积:V(CO2)=![]() ×22.4 L·mol-1=2.06 L。若9.2 g为两者混合物时,则有:2.06 L<V(CO2)<2.45 L。
×22.4 L·mol-1=2.06 L。若9.2 g为两者混合物时,则有:2.06 L<V(CO2)<2.45 L。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (K) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
 ,下列说法正确的是
,下列说法正确的是 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
已知天然气的主要成分 是一种会产生温室效应的气体,等物质够量的
是一种会产生温室效应的气体,等物质够量的 和
和 产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
①天然气与煤、柴油相比是较清洁的能源
②等质量的 和
和 产生的温室效应也是前者大
产生的温室效应也是前者大
③燃烧天然气也是酸雨的成因之一
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:013
已知天然气的主要成分 是一种会产生温室效应的气体,等物质够量的
是一种会产生温室效应的气体,等物质够量的 和
和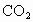 产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
①天然气与煤、柴油相比是较清洁的能源
②等质量的 和
和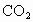 产生的温室效应也是前者大
产生的温室效应也是前者大
③燃烧天然气也是酸雨的成因之一
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com