
【题目】25℃时,0.1molL﹣1的HA溶液中c(H+)/c(OH﹣)=1010 . 请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是 (填字母).
A.c(H+)/c(HA) B.c(HA)/(A﹣) C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣)
③若M溶液是由上述HA溶液V1mL与pH=12的NaOH溶液V2mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+)+c(OH﹣)=2.0×10﹣7 molL﹣1
B.若V1=V2 , 则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2 .
【答案】弱电解质;B;AD
【解析】①25℃时,0.1molL﹣1的某酸HA中,如果该酸是强酸,氢离子浓度为0.1mol/L,氢氧根离子浓度为:10﹣13mol/L,则![]() =1012>1010 , 所以该酸是弱酸;所以答案是:弱电解质;
=1012>1010 , 所以该酸是弱酸;所以答案是:弱电解质;
②A.加水稀释促进了弱酸的电离,溶液中氢离子的物质的量增大,HA的物质的量减小,相同溶液中:![]() , 所以其比值增大,故A错误;
, 所以其比值增大,故A错误;
B.加水稀释促进酸电离,酸浓度、酸根离子浓度都降低,但酸根离子浓度减小的量小于酸分子减小的量,所以氢氧根离子浓度增大,则![]() 变小,故B正确;
变小,故B正确;
C.c(H+)与c(OH﹣)的乘积为水的离子积,温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,故D错误;
所以答案是:B;
③A.若混合溶液呈中性,则溶液M中c(H+)=c(OH﹣)=1×10﹣7 molL﹣1 , 所以溶液M中c(H+)+c(OH﹣)=2×10﹣7 molL﹣1 , 故A正确;
B.若V1=V2 , 则酸的浓度大,酸过量,则溶液M的pH一定小于7,故B错误;
C.如果溶液呈酸性,则溶液是酸和盐溶液,酸是弱酸,酸浓度大于氢氧化钠浓度,所以V1不一定大于V2 , 故C错误;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液,则V1一定小于V2 , 故D正确;
所以答案是:AD.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据图1给出的装置图回答下列问题: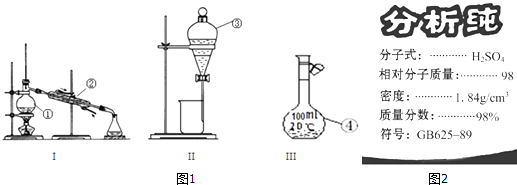
(1)写出下列玻璃仪器的名称:①;② .
(2)①~④中,使用前必须检查是否漏水的是(填仪器序号).分离溴水中的溴应先选择装置(填Ⅰ、Ⅱ或Ⅲ序号)
(3)图2为学校实验室买回的硫酸试剂瓶标签上的部分内容,现欲用此硫酸准确配制浓度为0.18molL﹣1的稀硫酸210mL.
①除量筒、烧杯、玻璃棒、胶头滴管等外,此实验还需要的主要仪器上图有无提供?(填“有”或“无”),如有,在下面横线上填写仪器序号(填①、②、③或④序号),如无,则填写需要怎样的主要仪器: .
②所量取的浓硫酸体积为mL.
③下列操作引起所配溶液浓度偏高的是 .
A.用相同装置配制过0.10mol/L的硫酸溶液后,未清洗即进行此实验的配制
B.移液时未对烧杯和玻璃棒进行洗涤
C.定容时仰视刻度线
D.颠倒摇匀后发现液面低于刻度线,但未加水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH,HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7 Ka2=4.7×10﹣11 |
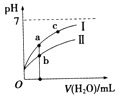
A.如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O═2HClO+CO32﹣
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液的叙述正确的是( )
A. 所有溶液都是无色的
B. 由分散质和分散剂组成的分散系一定是溶液
C. 均一稳定的液体是溶液
D. 溶液是由溶质和溶剂组成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a、b、c、d 4种金属两两连接浸入电解质溶液中,组成4个原电池(如图):
①中a极发生氧化反应 ②中电流由b到c ③中c极质量增加 ④中a极有大量气泡,则4种金属的活泼性由强到弱的顺序为( )
A.d>a>c>b
B.b>d>c>a
C.d>c>a>b
D.a>d>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4 , 请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有10mL、20mL、50mL量筒,应选用mL量筒,实验中用到的仪器除了烧杯、玻璃棒之外,还需要的仪器有:
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即转移到容量瓶
②定容时俯视刻度线
③所用过的烧杯、玻璃棒未洗涤 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,下列关于葡萄糖的说法错误的是( )
A. 葡萄糖是单糖B. 含有5个羟基(—OH)
C. 含有1个醛基(—CHO)D. 含有1个羧基(—COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。回答下列问题。
(1)久存的银制器皿表面会变黑,失去银白色的光泽,原因是。
(2)已知,Ksp=(AgCl)=1.8×10-10 , 若向50mL0.018mol/L的AgNO3溶液中加入50mL0.020mol/L的盐酸,混合后溶液中的Ag+的浓度为 mol/L,pH为 。
(3)AgNO3溶液光照易分解,生成Ag和红棕色气体等物质,其光照分解的化学方程式为 。
(4)右图所示原电池正极的反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com