
【题目】I.明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质,可利用明矾石制备氢氧化铝。
(1)已知明矾石脱水后要硫化,化学方程式为2Al2(SO4)3+3S![]() 2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是___________;若生成1 mol Al2O3,则转移的电子数为________。
2Al2O3+9SO2,该反应的氧化剂与还原剂的物质的量之比是___________;若生成1 mol Al2O3,则转移的电子数为________。
(2)证明废渣中含有Fe2O3 的化学方法:_____________________。
II.镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为:Mg17Al12 + 17H2=17MgH2 + 12Al ,得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。
(3)熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是_____________________
(4)在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为_______mol。(已知:MgH2 + 2HCl = MgCl2 + 2H2↑)
【答案】2:36NA (或3.612×1024)取少量废渣于试管,加入适量稀硫酸(或稀酸),溶解后滴加KSCN溶液,若溶液变红色,则证明废渣中含有Fe2O3 防止Mg、Al被空气氧化;52
【解析】I.(1)根据2Al2(SO4)3+3S![]() 2Al2O3+9SO2,反应中S是还原剂,Al2(SO4)3是氧化剂,氧化剂与还原剂的物质的量之比为2:3;反应中转移的电子数为12,若生成1 mol Al2O3,转移的电子6mol,数目为3.612×1024,故答案为:2:3;3.612×1024;
2Al2O3+9SO2,反应中S是还原剂,Al2(SO4)3是氧化剂,氧化剂与还原剂的物质的量之比为2:3;反应中转移的电子数为12,若生成1 mol Al2O3,转移的电子6mol,数目为3.612×1024,故答案为:2:3;3.612×1024;
(2)因含铁离子的溶液加KSCN溶液变为血红色可检验铁离子,选择HCl溶解固体,KSCN检验铁离子,则检验废渣中含有Fe2O3的方法为用盐酸溶解后滴加KSCN溶液,若溶液变红色,则证明废渣中含有Fe2O3,故答案为:用盐酸溶解后滴加KSCN溶液,若溶液变红色,则证明废渣中含有Fe2O3;
II.(3)镁、铝都是活泼的金属单质,容易被空气中的氧气氧化,通入氩气作保护气,以防止二者被氧化,故答案为:防止Mg Al被空气氧化;
(4)1molMg17Al12完全吸氢17mol,在盐酸中会全部释放出来,镁铝合金中的镁和铝都能与盐酸反应生成H2,生成氢气的物质的量分别为17mol、18mol,则生成氢气一共(17+17+12×![]() )mol=52mol,故答案为:52。
)mol=52mol,故答案为:52。


科目:高中化学 来源: 题型:
【题目】Ⅰ.已知:H2A的A2-可表示S2-、SO42-、SO32-、SiO32-或CO32-。
(1)常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液。有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。请根据图示填空:
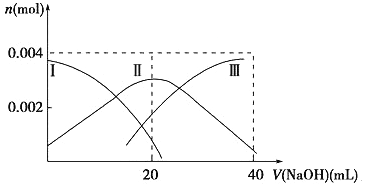
当V(NaOH)=20 mL时,溶液中离子浓度大小关系:____________。
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水____________(填“大”、“小”或“相等”)。
(2)若H2A为硫酸:t℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW=____________。
Ⅱ.已知:在25 ℃时 H2O![]() H++OH- KW=10-14
H++OH- KW=10-14
CH3COOH![]() H++CH3COO- Ka=1.8×10-5
H++CH3COO- Ka=1.8×10-5
(3)醋酸钠水解的平衡常数Kh具体数值=________________,
(4)0.5 mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a,1 mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为___________, a与b的关系为______________。(填“大于”“小于”或“等于”)
Ⅲ.(5)25 ℃时,将a mol·L-1的氨水与b mol·L-1盐酸等体积混合,反应后溶液恰好显中性,用a、b表示NH3·H2O的电离平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】氟及其氟产品在工农业生产中应用非常广泛,回答下列问题;
(l)基态氟原子核外电子的运动状态有______种,这些电子的电子云形状有_________种,氟原子的价电子排布式为______________。
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2晶体中所含作用力的类型有_______;与HF2-互为等电子体的分子有______(举一例)。
(3)三氟化硼乙醚(![]() )熔点-58℃,沸点126~129℃,它属于_____________晶体。
)熔点-58℃,沸点126~129℃,它属于_____________晶体。
(4)氟化钙晶胞结构如下图所示,晶胞参数a=0.555 nm。
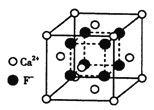
①Ca2+、F-的配位数分别为___________和___________。
②列式表示氟化钙晶体的密度________g/cm3(不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等体积、等物质的量浓度的NH3HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.![]() <1.0×10-7mol·L-1
<1.0×10-7mol·L-1
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D.c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列金属的熔沸点:
金属 | Na | Cu | Al | Fe |
熔点(℃) | 97.5 | 1083 | 660 | 1535 |
沸点/℃ | 883 | 2595 | 2200 | 3000 |
不能形成合金的两金属是( )
A.Cu与Na
B.Fe与Cu
C.Fe与Al
D.Al与Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学选修3—物质结构与性质】
A、B、W、D、L为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)W2-离子的结构示意图为__________,E元素在周期表中的位置为_________,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式____________________。
(2)经测定A2W2为二元弱酸,A2W2的电子式为____________,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式___________________。
(3)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成,当消耗2molI-时,共转移3mol电子,该反应的离子方程式是________________。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,写出该反应方程式_____________,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_____________L(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com