
����Ŀ��������Ҫ�Ľ������ϣ�������(��Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����)�ǹ�ҵ����ȡ����ԭ�ϡ�ʵ����ģ�ҵ����������Ϊԭ����ȡAl2(SO4)3�����������[NH4Al(SO4)2��12H2O]�Ĺ���������ͼ��ʾ��
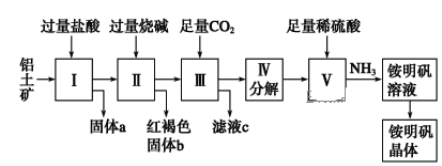
��ش��������⣺
��1������a�Ļ�ѧʽΪ________��
��2��д�����мӹ������ռ��漰���ķ�Ӧ���ӷ���ʽ______________��_____________������ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ_________________��
��3���ɢ��еõ���Һc��ʵ�����Ϊ__________�����������Һ�л������������ʵ���������Ϊ(���������)________����ȴ�ᾧ������ϴ�ӡ�
��4����Һc��________�ԣ��ճ������г�����������________________����дһ�㣩��
��5���������NH4Al(SO4)2�м���������ʹ�����������ȫ������ѧ����ʽΪ_____________��
���𰸡�SiO2Al3+ +4OH-=AlO2��+2H2OFe3+ +3OH-=Fe(OH)3��AlO2����CO2��2H2O=HCO3����Al(OH)3����������Ũ����ͷ�2Ba(OH)2+NH4Al(SO4)2=2BaSO4��+NH3��H2O+Al(OH)3��
��������
�������������ܽ⣬Al2O3��Fe2O3�����ᷴӦ�õ�AlCl3��FeCl3��SiO2�������ᷴӦ�����˵õ�����aΪSiO2����Һ�к���AlCl3��FeCl3��ʣ���HCl���ټ���������ռ��Ӧ�õ���������������ƫ�����ơ��Ȼ��ƣ����ˣ����ɫ����bΪ������������Һ���к���ƫ�����ơ��Ȼ��Ƽ�ʣ���NaOH��ͨ������Ķ�����̼����Ӧ������������������̼�����ƣ����ˣ���Һc�к����Ȼ��ơ�̼�����ƣ����������ȷֽ�õ����������������ܽ�õ���������Һ����ͨ�백�����õ��������Һ���������Ũ������ȴ�ᾧ�����˵Ȳ����õ���������塣
��1����������Al2O3��Fe2O3���������ᣬSiO2���������ᣬ���Թ���a�Ļ�ѧʽΪSiO2����2������FeCl3��AlCl3����Һ�м��������NaOH��Һ�������ķ�Ӧ�õ�Fe(OH)3���ɫ������ƫ��������Һ����Ӧ�����ӷ���ʽΪ��Fe3����3OH-��Fe(OH)3����Al3����4OH-��AlO2-+2H2O��������Һ��ͨ�������CO2���õ�Al(OH)3��ɫ������HCO3������Ӧ�����ӷ���ʽ�ǣ�AlO2����CO2��2H2O=HCO3����Al(OH)3������3��������I��II��III�����ڹ����Һ��ķ��룬Ӧ�ù��˵ķ��������������Һ�л������������ʵ���������Ϊ����Ũ������ȴ�ᾧ������ϴ�ӡ���4����Һc�к����Ȼ��ơ�̼�����ƣ�̼����������Һ��ˮ�⣬��Һ�Լ��ԣ��ճ������У�̼�����ƿ��������ͼ�����ĭ��������5���������NH4Al(SO4)2�м���������ʹ�����������ȫ�������õ����ᱵ��������������������һˮ�ϰ�����Ӧ�Ļ�ѧ����ʽΪ2Ba(OH)2+NH4Al(SO4)2=2BaSO4��+NH3��H2O+Al(OH)3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������dz��õ�����������ҵ�������̿�(��Ҫ�ɷ���MnO2)Ϊԭ���Ʊ�������ؾ��塣�м����Ϊ����ء���ͼ��ʵ����ģ���Ʊ�KMnO4����IJ������̣�
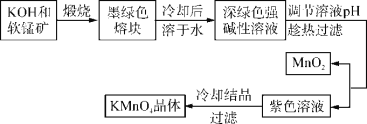
��֪�������(K2MnO4)��ī��ɫ���壬��ˮ��Һ������ɫ���������������(MnO![]() )��ˮ��Һ�е�������ɫ����ǿ������Һ�����ȶ����ڣ������ԡ����Ժ������Ի����£�MnO
)��ˮ��Һ�е�������ɫ����ǿ������Һ�����ȶ����ڣ������ԡ����Ժ������Ի����£�MnO![]() �ᷢ������������ԭ��Ӧ������MnO
�ᷢ������������ԭ��Ӧ������MnO![]() ��MnO2��
��MnO2��
�ش��������⣺
(1)KOH�ĵ���ʽΪ____________��
(2)������ҺpH�����У��������������뻹ԭ��������ʵ���֮��Ϊ____________��
(3)���ȹ��˵�Ŀ����_____________________________________________��
(4)��֪20 ��ʱK2SO4��KCl��CH3COOK���ܽ�ȷֱ�Ϊ11.1 g��34 g��217 g����������Ϸ�����ѡ����������________(����)���õ��ĸ�����ؾ��崿�ȸ��ߡ�
A��ϡ���� B��Ũ���� C������ D��ϡ����
(5)��Ʒ��KMnO4�Ķ���
������Ũ��Ϊ0.1250 mg�� mL��1��KMnO4����Һ100 mL��
�ڽ�������Һϡ��ΪŨ�ȷֱ�Ϊ2.5��5.0��7.5��10.0��12.5��15.0(��λ��mg��L��1)����Һ���ֱ�ⶨ��ͬŨ����Һ�Թ�����ճ̶ȣ������ⶨ������Ƴ��������¡�

�۳�ȡKMnO4��Ʒ(����K2MnO4)0.1250 g���������ò�Ʒ��Һ1000 mL��ȡ10 mLϡ����100 mL��Ȼ����ڵķ������вⶨ�����βⶨ���õ�����ȷֱ�Ϊ0.149��0.151������Ʒ��KMnO4����������Ϊ________��
(6)����KMnO4��Һ��FeSO4��Һ��Ӧ�����ӷ���ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��֤�����������۵��������д��ʵ�鲽�������_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ�ϵ����Ŀǰ����о����ȵ�֮һ������ij����С�����Ƶ�����ȼ�ϵ�أ���ͼ��ʾ��a��b��Ϊ���Ե缫��������������ȷ����(����)

A��a�����������õ缫�Ϸ���������Ӧ
B��b����Ӧ��O2��4OH����4e��===2H2O
C���ܷ�Ӧ����ʽΪ2H2��O2===2H2O
D������ȼ�ϵ����һ�־���Ӧ��ǰ������ɫ��Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���A��B��C�������ʸ�1 molͨ��һ���ܱ������з�����Ӧ��2A��B![]() 2C���ﵽ��ѧ��Ӧ��ʱ��B�����ʵ���������(����)
2C���ﵽ��ѧ��Ӧ��ʱ��B�����ʵ���������(����)
A. 1.5 molB. 1 molC. 0.5 molD. 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʫ�䡢������뻯ѧ�����йأ�˵������ȷ����
A. ��ˮ�齻�ڣ����Ͻ�����ǰ�߰��������仯�������߰�����ѧ�仯
B. �������з�ź������϶������˻�ѧ�仯
C. ����ˮʯ��������ľ������������ѧ�仯
D. �����Ʒ�ƽ�˾���ʵ����ӿ����������������ܽ�ƽ���״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��5��9��,���·��ֵĵ�113�š�115�š�117�ź�118��Ԫ������������������

����Ԫ��������֪ʶ,����Ԥ���˵���϶������������� ��
A. Nh������������Ӧ��ˮ����Ļ�ѧʽΪH3NhO3��һ��ǿ��
B. Mc�����������ΪMc5+,�����ԱȽ���
C. Og�ǵ��������е����һ��Ԫ��,��ԭ�������������ѷ���Ԫ��������
D. ���ݽ����ͷǽ����ķֽ���,Ts����������Ϊ���䡱���ܸ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʺ��еĻ�ѧ��������ȫ��ͬ���ǣ�
A. NaOH��CaCl2��CaO B. Na2O��Na2O2��Na2S
C. NaCl��HCl��H2O D. HBr��CO2��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������(��Ҫ�ɷ�ΪAl2O3����Fe2O3����)Ϊԭ��ұ�����Ĺ���������ͼ��ʾ��
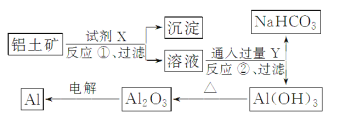
����������ȷ����
A. �Լ�X������NaOH��Һ��Ҳ����������
B. ��Ӧ�ٹ��˺����ó���ΪFe(OH)3
C. ͼ������ת����Ӧ������������ԭ��Ӧ
D. ��Ӧ�ڵĻ�ѧ����ʽΪNa[Al(OH)4]��CO2===Al(OH)3����NaHCO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com