
以黄铜矿(CuFeS2)为原料冶炼铜的反应为:
8CuFeS2 +21O2 8Cu +4FeO+2Fe2O3 + 16SO2
8Cu +4FeO+2Fe2O3 + 16SO2
(1)若Cu为+2价,则反应中每生成1 mol Cu需要转移____________ mol 电子。
(2)为综合利用炉气中的大量SO2,下列方案合理的是____________。
a.用浓硫酸吸收
b.用于制备硫酸
c.高空排放
d.用纯碱溶液吸收制亚硫酸钠
(3)为检验所得矿渣中是否含有FeO、Fe2O3、CuO、Al2O3、SiO2 等氧化物,进行了以下实验:
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通人品红溶液中,溶液褪色。由此判断矿渣中一定含有_________ ,一定没有_________。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH 溶液,有沉淀产生,静置后取上层清液,通入过量的CO2, 溶液变浑浊。由此判断出矿渣中一定含有____________ ,写出通入过量的CO2所发生反应的离子方程式:_________________ 。
③另取一份溶液A加入过量的铁粉,充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有_____________ , 写出此步操作中得到红色物质所发生反应的离子方程式__________________。
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
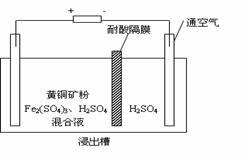 (8分)以石墨为电极,电解法处理黄铜矿(CuFeS2)精矿,可以制得硫酸铜溶液和单质硫。黄铜矿在阳极的浸出反应比较复杂,主要有:
(8分)以石墨为电极,电解法处理黄铜矿(CuFeS2)精矿,可以制得硫酸铜溶液和单质硫。黄铜矿在阳极的浸出反应比较复杂,主要有:
CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S,
CuFeS2 + 4Fe3+ = Cu2+ + 5Fe2+ + 2S,
2Fe3+ + H2S = 2H+ + S↓ + 2Fe2+。右图为该工艺的示意图。
(1)电解过程实现了Fe3+的循环,则阳极方程式为 ▲ 。
(2)电解过程中阴极析出的金属为 ▲ ,向阴极通空气的原因是 ▲ 。
(3)与燃烧法炼铜相比,电解法的优点为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com