
甲、乙、丙、丁、戊均为中学化学中常见的单质或化合物,且均含有同一种元素R,在一定条件下其转化关系如图所示。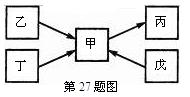
(1)若R为一种非金属元素,且上述五种物质含右不同的官能团,丁为带水果香味的液体,乙和丁均能在碱性条件下生成甲,戊是一种无色气体,相同条件下戊相对H2的密度为14。
写出由甲生成戊的化学方程式 ,欲检验乙中官能团,所选用的试剂为(填序号) 。
①NaOH溶液 ②Br2的CCl4溶液 ③银氨溶液 ④AgNO3溶液 ⑤稀HNO3
(2)若R为另一种非金属元素;甲与丙为常见大气污染物,且甲与丙的相对分子质量之差为1 6。丁为空气的主要成分之一。则丁的电子式为 ,乙的空间构型为 。戊的稀溶液能跟过量铁粉反应,其离子反应方程式为 。
6。丁为空气的主要成分之一。则丁的电子式为 ,乙的空间构型为 。戊的稀溶液能跟过量铁粉反应,其离子反应方程式为 。
(3)若R为一种金属元素,甲溶液的pH小于7,乙由两种元素组成,单质丁在二定条件下可生成戊。甲与戊两种溶液混合能生成沉淀丙,其离子方程式为 ,若镁粉中混有少量的丁,除去丁的离子方程式为 。
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:阅读理解
| ② | |||
| ⑦ | ⑧ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
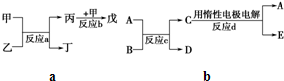
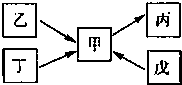 甲、乙、丙、丁、戊均为中学化学常见的单质或化合物,且均含有同一种元素R,在一定条件下其转化关系如图所示.
甲、乙、丙、丁、戊均为中学化学常见的单质或化合物,且均含有同一种元素R,在一定条件下其转化关系如图所示.| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
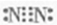
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| ② | |||
| ⑦ | ⑧ |
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com