
| A.太阳能 | B.石油 | C.天然气 | D.煤 |
科目:高中化学 来源:不详 题型:单选题
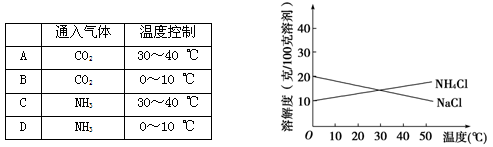
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁 |
| C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| D.炼铜:用黄铜矿(主要成分为CuFeS2)直接电解精炼得到纯度为99.9%的铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用潮汐发电,将化学能转化为电能 | B.不需富集,直接提取海水中的溴 |
| C.用海水中的NaCl制取烧碱和纯碱 | D.只需使海水中的碘升华就能得到碘单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
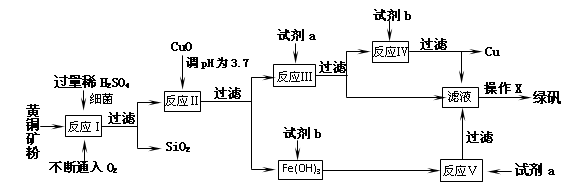
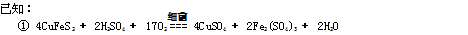
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
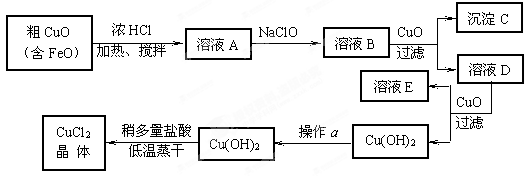
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验中包含溶解、过滤、升华等步骤 |
| B.加入过量的氯水将I-全部氧化成I2 |
| C.可以用CCl4直接将海带中的碘元素萃取出来 |
| D.将海带灼烧的目的是除掉其中的有机物,将碘元素转化为I- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
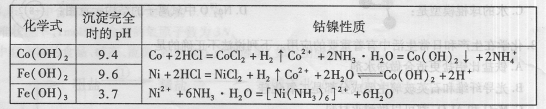
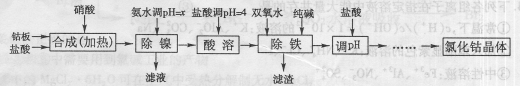
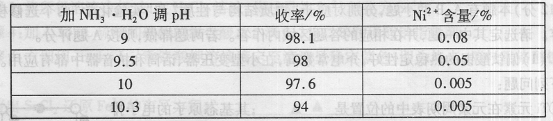
 Fe(OH)3+3H+的平衡常数为 。
Fe(OH)3+3H+的平衡常数为 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com