
【题目】制取漂白粉的化学方程式是:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应的氧化剂与还原剂之比为
A.1:2 B.2:1 C.1:1 D.3:2
科目:高中化学 来源: 题型:
【题目】下列离子可以大量共存的是
A. K+ SO42- Na+ HCO3- B. K+ Ag+ Cl- NO3-
C. Ba2+ Na+ OH- CO32- D. Al3+ NH4+ NO3- OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( ) 
A.原子半径:Z>W>X>Y
B.气态氢化物的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值不可能相等
D.Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A. 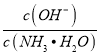 B.
B. 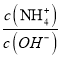 C.
C. 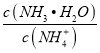 D. c(OH-)
D. c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列开发利用自然资源制取化学品,其简示途径较为合理的是( )
A.海水 ![]()
![]() Br2
Br2
B.海产品(如海带等) ![]()
![]() 滤液
滤液 ![]()
![]()
![]() I2
I2
C.海水 ![]() Mg(OH)2
Mg(OH)2 ![]() MgO
MgO ![]() Mg
Mg
D.铝土矿 ![]() 滤液
滤液 ![]() Al(OH)3
Al(OH)3 ![]()
![]() Al
Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是
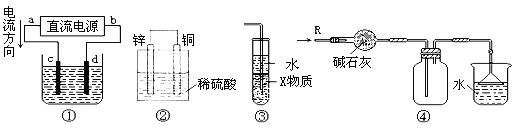
A. 若采用装置①铝件镀银,则c极为铝件,d极为纯银,电解质溶液为AgNO3溶液
B. 装置②是原电池,能将化学能转化为电能,SO42-移向锌电极
C. 装置③中X若为四氯化碳,用于吸收氨气或氯化氢,会引起倒吸
D. 装置④可用于收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b代表2种金属,下列叙述中,肯定能判断金属活动性a比b强的是( )
A. 常温下,a能从水中置换出氢,而b不能 B. 原子的电子层数a比b多
C. 原子的最外层电子数a比b少 D. 1 mol a 、b分别与足量盐酸反应,生成H2的质量a比b大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
![]()
试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子方程式为_________________;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有__________、玻璃棒和烧杯等;步骤Ⅳ中最好应选用_______试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氧化铜 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是_____________________;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是______________________;
(5)步骤Ⅵ中发生反应的化学反应方程式为_______________________________;
(6) 欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com