
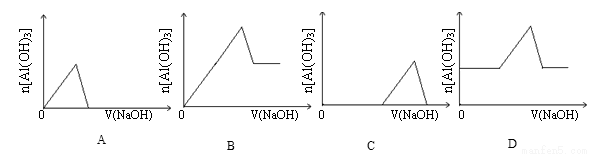
已知室温下,Al(OH)3的溶解度远大于Fe(OH)3。向浓度均为0.1mol·L—1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年吉林省高一下期末化学试卷(解析版) 题型:选择题
下列排列有错误的是
A.粒子半径:Al3+>Mg2+>Na+>F-
B.稳定性:HF>HCl>HBr>HI
C.酸性:H4SiO4<H3PO4<H2SO4<HClO4
D.碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:选择题
在100g碳不完全燃烧所得气体中,CO占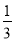 ,CO2占
,CO2占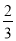 ,且C(s)+
,且C(s)+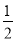 O2(g) =CO(g),△H=-110.35kJ/mol;CO(g)+
O2(g) =CO(g),△H=-110.35kJ/mol;CO(g)+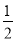 O2(g)=CO2(g),△H=-282.57 kJ/mol,与这些碳完全燃烧相比,损失的热量是
O2(g)=CO2(g),△H=-282.57 kJ/mol,与这些碳完全燃烧相比,损失的热量是
A.392.92kJ B.2489.44kJ
C.784.92kJ D.3274.3kJ
查看答案和解析>>
科目:高中化学 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:填空题
(8分)镁是海水中含量较多的金属元素,单质镁、镁合金以及镁的化合物在科学研究和工业生产中用途非常广泛.
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1== -74.5kJ/mol
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2== -64.4kJ/mol
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3
则ΔH3== kJ/mol
(2)工业上可用电解熔融的无水氯化镁获得镁.其中氯化镁晶体脱水是关键的工艺之一.一种正在试验的氯化镁晶体脱水的方法是:先将MgCl2•6H2O转化为MgCl2•NH4Cl•nNH3,然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为 ;用惰性电极电解熔融氯化镁,阴极的电极反应式为 。
(3)储氢材料Mg(AlH4)2在110℃﹣200℃的反应为:Mg(AlH4)2===MgH2+2Al+3H2↑,每生成27gAl转移电子的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第一次精英对抗赛化学试卷(解析版) 题型:选择题
足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50 mL,下列说法正确的是 ( )
A.参加反应的硝酸是0.4mol B.混合气体中含NO21.12 L
C.此反应过程中转移的电子为0.3 mol D.消耗氧气的体积为1.68 L
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期第二次质量检测考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀。
B.2NO(g)+2CO(g) N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0。
N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0。
C.加热0.1 mol·L-1 Na2CO3溶液,CO32-水解程度和溶液的pH均增大。
D.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大。
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则地区一中高三10月月考理综化学试卷(解析版) 题型:填空题
(13分)工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质,并用来生产ZnSO4·6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的pH如下表。

氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 8.0 |
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有________。
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是_____。为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为______。为控制上述pH范围可选择加入的试剂或药品是________。
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是_______。“操作A”的名称是_______。
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于___________。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
根据表中信息判断,下列选项正确的是

A.第①组反应的其余产物为H20
B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1:2
C.第③组反应中生成1 mol Cl2,转移电子5 mol
D.氧化性由强到弱顺序为Mn04->Cl2 >Fe3+>Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com