
常温下,下列溶液中各组离子一定能大量共存的是
A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO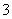 、CO
、CO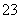
B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl-
C.含有0.1 mol·L-1 HCO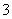 的溶液:Na+、Fe3+、NO
的溶液:Na+、Fe3+、NO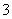 、SCN-
、SCN-
 D. =0.1 mol·L-1的溶液:Na+、K+、CO
D. =0.1 mol·L-1的溶液:Na+、K+、CO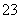 、NO
、NO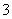
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2(g)+O2(g) 2SO3(g) △H<0
2SO3(g) △H<0
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0
4NO(g)+6H2O(g) △H<0
C.H2(g)+I2(g) 2HI(g) △H>0
2HI(g) △H>0
D.C(s)+H2O(g) CO(g)+H2(g) △H>0
CO(g)+H2(g) △H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
将Cu片放入0.1 mol·L-1 FeCl3溶液中,反应一定时间后取出Cu片,溶液中c (Fe3+)∶c (Fe2+)=2∶3,则Cu2+与Fe3+的物质的量之比为( )
A.3∶2 B.3∶5 C.4∶3 D.3∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是还原性铁粉与水蒸气反应的实验装置图,实验时,B中灰色的铁粉变为黑色,且生成的黑色固体物质是一种可溶于稀盐酸的较复杂化合物。请回答下列问题:
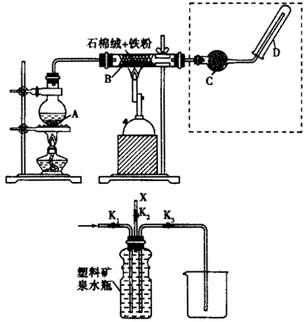
(1)B中发生反应的化学方程式为________。
(2)反应前向A中投放碎瓷片的目的是________。
(3)某次实验后,取少量B中的固体物质,溶于足量稀盐酸,再滴加KSCN溶液。溶液颜色无明显变化,试解释原因________。
(4)图中虚线部分,可以用图中下面所示装置代替,在X口点燃收集到的气体即可检验H2的存在。实验开始时,打开K1、K2,关闭K3,使反应先进行一段时间之后,必须进行________操作,方可关闭K2,打开K3,再收集气体。当收集到半瓶气体时,停止加热,关闭K1,若要使H2顺利逸出而进行点燃实验,操作的方法是________。
(5)替代装置未像原装置那样使用干燥管,同样顺利完成了实验,原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z的原子序数依次增大,且原子最外层电子数之和为14。X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最高的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
A.元素X的最高价氧化物对应的水化物的酸性比Z的弱
B.元素Y、Z的简单离子的电子层结构相同
C.元素W与Z形成的化合物为离子化合物
D.原子半径由大到小的顺序为:r(Z)>r(Y)>r (W)
查看答案和解析>>
科目:高中化学 来源: 题型:
向2.0 L恒容密闭容器中充入1.0 mol PCl5,在温度为T℃时发生如下反应PCl5(g)  PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题: [已知:Ksp(Ag3 PO4) =1.4 × 10-16,Ksp(AgCl) =1.8 × 10-10]
(1)反应在前50 s的平均速率v(PCl5) = ▲ 。
(2)温度为T℃时,该反应的化学平衡常数= ▲ 。
(3)要提高上述反应的转化率,可采取的措施是 ▲ (任写一种)。
(4)在温度为T℃时,若起始时充入0.5 mol PCl5和a mol Cl2,平衡时PCl5的转化率仍为20%,则a= ▲ 。
(5)PCl5在热水中完全水解生成H3 PO4,该反应的化学方程式是 ▲ 。 若将0.01 mol PCl5投入l L热水中,再逐滴加入0.1 mol /L AgNO3溶液,先产生的沉淀是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
(1)铜钱在我国历史上曾经是一种广泛流通的货币,铜常用于制造货币的原因可能是________(填序号)。
A.铜的熔点不是太高,易于冶炼铸造成型 B.铜的性质不活泼,不易被腐蚀
C.我国较早掌握了湿法冶炼铜的技术 D.自然界有大量游离态的铜
(2)钢铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是________(填名称),铁的氧化物常见的还有________(填化学式)。
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用。但是该氧化膜易被酸、碱破坏,若用铝制品盛放氢氧化钠溶液,发生反应的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com