
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
(1)铜钱在我国历史上曾经是一种广泛流通的货币,铜常用于制造货币的原因可能是________(填序号)。
A.铜的熔点不是太高,易于冶炼铸造成型 B.铜的性质不活泼,不易被腐蚀
C.我国较早掌握了湿法冶炼铜的技术 D.自然界有大量游离态的铜
(2)钢铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是________(填名称),铁的氧化物常见的还有________(填化学式)。
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用。但是该氧化膜易被酸、碱破坏,若用铝制品盛放氢氧化钠溶液,发生反应的化学方程式为________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是
A.KClO3是氧化剂
B.被氧化与被还原的氯元素的质量比为5:1
C.H2SO4既不是氧化剂又不是还原剂
D.1mol KClO3参加反应时有10mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列溶液中各组离子一定能大量共存的是
A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO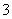 、CO
、CO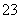
B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl-
C.含有0.1 mol·L-1 HCO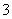 的溶液:Na+、Fe3+、NO
的溶液:Na+、Fe3+、NO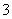 、SCN-
、SCN-
 D. =0.1 mol·L-1的溶液:Na+、K+、CO
D. =0.1 mol·L-1的溶液:Na+、K+、CO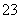 、NO
、NO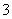
查看答案和解析>>
科目:高中化学 来源: 题型:
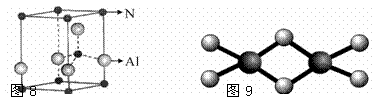
用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料,氮化铝(其晶胞如图8所示)可由氯化铝与氨经气相反应制得。
 |
(1)基态Cr的价电子排布式可表示为 ▲ 。
(2)氮化铝的化学式为 ▲ ,距离铝原子最近且距离相等的氮原子数目为 ▲ 个。
(3)氯化铝易升华,其双聚物Al2Cl6结构如图9所示。在Al2Cl6中存在的化学键有 ▲ (填字母)。
a.离子键 b.共价键 c.配位键 d.金属键
(4)一定条件下用Al2O3和CCl4反应制备AlCl3的反应为:Al2O3+3CCl4===2AlCl3+3COCl2。其中COCl2分子的空间构型为 ▲ 。一种与CCl4互为等电子体的分子的化学式为 ▲ 。
(5)AlCl3在下述反应中作催化剂。分子③中碳原子的杂化类型为 ▲ 。
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体,下列区分这两种物质的方法中正确的是( )
A.分别用砂锅加热两种样品,全部分解挥发没有残留物的是小苏打
B.用洁净的铁丝蘸取两种样品在煤气灯火焰上灼烧,使火焰颜色发生明显变化的是小苏打
C.用两只小玻璃杯,分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是纯碱
D.先将少量两种样品配成溶液,分别加入氯化钙溶液,无白色沉淀生成的是小苏打
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列热化学方程式:H2(g)+1/2O2(g)== H2O(l) △H= -285.8kJ/mol,
H2(g)+1/2O2(g)== H2O(g) △H= -241.8kJ/mol则氢气的标准燃烧热是
A.-285.8kJ/mol B. 285.8kJ/mol C. -241.8kJ/mol D. 241.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.金属腐蚀就是金属原子失去电子被还原的过程
B.合金都比纯金属易被腐蚀
C.将金属与外加直流电源的负极相连,而将正极接到废铁上,可以防止金属被腐蚀
D.钢铁设备上连接铜块可以防止钢铁被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
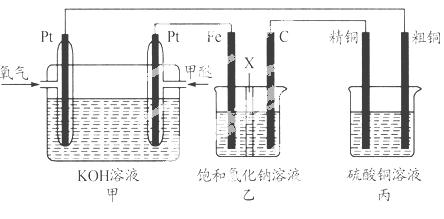
根据要求回答相关问题:
(1)通入氧气的电极为________(填“正极”或“负极”),写出负极的电极反应式_______________________________。
(2)铁电极为________(填“阳极”或“阴极”),石墨电极(C)的电极反应式为________________________________________。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________(填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为______ ___ __,反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的标况下的体积为____ ____;丙装置中阴极析出铜的质量为____ ___ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
在0℃和1.01×105 Pa条件下,将0.1 g H2、3.2 g SO2、2.2 g CO2混合,该混合气的体积是
A.2.24 L B.3.36 L
C.4.48 L D.6.72 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com