
【化学一有机化学基础】(15分)直接生成碳-碳键的反应是实现高效、绿色有机合成的重要途径。交叉脱氢偶联反应是近年备受关注的一类直接生成碳-碳键的新反应。例如:

化合物Ⅰ可由以下合成路线获得:

(1)化合物Ⅰ的分子式为___________,其在NaOH溶液中水解的化学方程式为_____。
(2化合物Ⅱ与足量浓氢溴酸反应的化学方程式为_________________________________。
(3化合物Ⅲ没有酸性,其结构简式为___________________;Ⅲ的一种同分异构体Ⅴ能与饱和NaHCO3溶液反应放出CO2,化合物Ⅴ的结构简式为______________________________。
(4)反应①中1个脱氢剂Ⅵ(结构简式如 )分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为________________________。
)分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为________________________。
(5)1分子 与1分子
与1分子 在一定条件下可发生类似反应①的反应,其产物分子的结构简式为______________________;1mol该产物最多可与______molH2发生加成反应。
在一定条件下可发生类似反应①的反应,其产物分子的结构简式为______________________;1mol该产物最多可与______molH2发生加成反应。
(1)C5H8O4 (1分) H3COOCCH2COOCH3+2NaOH 2CH3OH+NaOOCCH2COONa(2分)(2)HOCH2CH2CH2OH+2HBr
2CH3OH+NaOOCCH2COONa(2分)(2)HOCH2CH2CH2OH+2HBr CH2BrCH2CH2Br+2H2O(2分)
CH2BrCH2CH2Br+2H2O(2分)
(3)OHCCH2CHO(2分) CH2=CHCOOH(2分)
(4)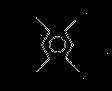 (2分)(5)
(2分)(5) (2分)8(2分)
(2分)8(2分)
【解析】
试题分析:(1)根据化合物的结构简式可知化合物Ⅰ的分子式为C5H8O4,分子中含有2个酯基,则其在NaOH溶液中水解的化学方程式为H3COOCCH2COOCH3+2NaOH 2CH3OH+NaOOCCH2COONa。
2CH3OH+NaOOCCH2COONa。
(2)Ⅳ与甲醇发生酯化反应生成I,则Ⅳ的结构简式为HOOCCH2COOH。Ⅲ发生银镜反应生成Ⅳ,则Ⅲ的结构简式为OHCCH2CHO,Ⅱ发生催化氧化生成Ⅲ,则Ⅲ的结构简式为HOCH2CH2CH2OH。醇与溴化氢发生取代反应的方程式为HOCH2CH2CH2OH+2HBr CH2BrCH2CH2Br+2H2O。
CH2BrCH2CH2Br+2H2O。
(3)根据以上分析可知Ⅲ的结构简式为HOCH2CH2CH2OH。Ⅲ的一种同分异构体Ⅴ能与饱和NaHCO3溶液反应放出CO2,说明分子中含有羧基,因此根据分子式可知一定还含有碳碳双键,则化合物Ⅴ的结构简式为CH2=CHCOOH。
(4)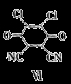 分子获得2个氢原子后,转变成1个芳香族化合物分子,这说明分子中含有苯环,则碳氧双键均变为酚羟基,因此该芳香族化合物分子的结构简式为
分子获得2个氢原子后,转变成1个芳香族化合物分子,这说明分子中含有苯环,则碳氧双键均变为酚羟基,因此该芳香族化合物分子的结构简式为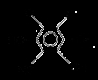 。
。
(5)反应①属于取代反应形成碳碳单键,则1分子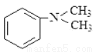 与1分子
与1分子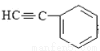 在一定条件下发生类似反应①的反应,其产物分子的结构简式为
在一定条件下发生类似反应①的反应,其产物分子的结构简式为 。该化合物分子中含有2个苯环、1个碳碳三键,所以1mol该产物最多可与8molH2发生加成反应。
。该化合物分子中含有2个苯环、1个碳碳三键,所以1mol该产物最多可与8molH2发生加成反应。
考点:考查有机物推断、同分异构体判断以及方程式书写等


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2014-2015学年甘肃省高三上学期期末理综化学试卷(解析版) 题型:推断题
(选考)【化学——有机化学基础】(15分)
有机物A是常用的食用油抗氧化剂,分子为C10H12O5,可发生如下变化:
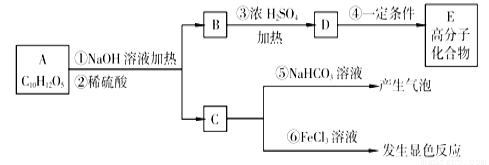
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为: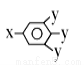 (其中-x、-y均为官能团)。请回答下列问题:
(其中-x、-y均为官能团)。请回答下列问题:
(1)根据系统命名法B的名称为 。
(2)官能团-x的名称为 ,高聚物E的链节为 。
(3)A的结构简式为 。
(4)反应⑤的化学方程式为 。
(5)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式 、 。
①含有苯环 ②能发生银镜反应 ③含有酚羟基
(6)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号)。
A.含有苯环 B.含有羰基 C.含有酚羟基
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省名校新高考研究联盟高三上学期联考化学试卷(解析版) 题型:选择题
铁氧体(Fe3O4)法是处理含铬废水的常用方法,其原理是:用FeSO4把废水中Cr2O 还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物
还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物 。处理含1 mol Cr2O
。处理含1 mol Cr2O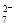 废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
A.x=0.5,a=10 B.x=1,a=5
C.x=2,a=10 D.x=0.5,a=8
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省红河州高三统一检测理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】(15分)
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道。请回答下列问题:
(1)R原子的基态电子排布式为 。
(2)X、Y原子的第一电离能大小顺序为 。(用元素符号表示)
(3)X的常见单质分子结构中σ键数目为 。
(4)Z的最高价氧化物对应水化物的酸根离子空间构型为 ,中心原子的杂化轨道类型为 。
(5)某矿物晶体由Y、W、R三种元素组成,其晶胞结构如图所示。

则该矿物的化学式为 ,若已知该晶胞的边长为a cm,则该晶胞的密度为 g/cm3。(用含a、NA的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省红河州高三统一检测理综化学试卷(解析版) 题型:选择题
下图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是:

A.分子组成为Cm(H2O)n的物质一定是糖类
B.微生物所在电极区放电时发生还原反应
C.放电过程中,H+从正极区移向负极区
D.正极反应式为:MnO2+4H++2e—=Mn2++2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省部分高三1月份统一考试理综化学试卷(解析版) 题型:填空题
(14分)I.氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(图中涉及物质为气态)

(1)上图是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_________________________________________。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请完成下列问题。
①试比较K1、K2的大小,K1___________K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是______________(填序号字母):
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得NH3和N2、H2的物质的量分别为1mol和2mol、3mol时,则该反应的v(N2)正______________v(N2)逆(填写“>”、“=”或“<”)。
II.描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)。
酸或碱 | 电离平衡常数(Ka或 Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3·H2O | 1.8×10-5 |
请回答下列问题:
(1)上述四种酸中,酸性最弱的是_________________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是_________________(填序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈____(选填“酸性”“中性”或“碱性”),理由是:__________________________,溶液中各离子浓度大小的关系是__________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省部分高三1月份统一考试理综化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列说法正确是
A.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2
B.向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染
C.高纯度的硅单质广泛用于制作光导纤维
D.大量燃烧化石燃料排放的废气中含CO2、SO2,从而使雨水的pH=5.6形成酸雨
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市崇明县高三上学期期末考试化学试卷(解析版) 题型:选择题
C60可用作储存氢气的材料,结构如右图所示。继C60后,科学家又合成了Si60、N60,三种物质结构相似。下列有关说法正确的是

A.C60、Si60、N60都属于原子晶体
B.C60、Si60、N60分子内共用电子对数目相同
C.由于N-N键能小于N≡N,故N60的稳定性弱于N2
D.由于 键长小于
键长小于 键,所以C60熔沸点低于Si60
键,所以C60熔沸点低于Si60
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省滕州市上学期高三第四次月考理综化学试卷(解析版) 题型:实验题
(16分)
Ⅰ.实验室常见的几种气体发生装置如图A、B、C所示:

(1)实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为_____________________________ ____。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是_______________(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的________。
①CO2 ②NO ③Cl2 ④H2 ⑤HCl
其中在D装置中连接小烧杯的目的是____________________。
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
(1)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为________,制备X的化学方程式为______________________________________;
(2)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。

氨的测定装置(已省略加热和夹持装置)
①装置中安全管的作用原理是__________________________________________。
②样品中氨的质量分数表达式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com