
【题目】向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)
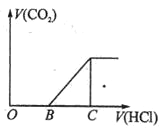
A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
【答案】C
【解析】
向某NaOH溶液中通入CO2气体,涉及反应及产物分别为:2NaOH+CO2=Na2CO3+H2O(CO2+2OH-=CO32-+H2O);NaOH+CO2=NaHCO3(OH―+CO2═HCO3―);M溶液加入盐酸时发生的反应可能为:CO32-+H+=HCO3-,HCO3-+H+=H2O+CO2↑;在不同的物质的量比的范围内产物(溶液M的成份)不同,参见下图:设a=n(CO2)/n(NaOH),则:
a | M的成分 | OB与BC的关系 |
a<1:2 | NaOH 和 Na2CO3 | OB>BC |
a=1:2 | Na2CO3 | OB=BC |
1:2<a<1:1 | NaHCO3和Na2CO3 | OB<BC |
a≥1:1 | NaHCO3 | OB=0 |
由上表可知,若3OB=BC,则溶液M的成分为NaHCO3和Na2CO3,可得:3n(Na2CO3)=n(Na2CO3)+n(NaHCO3)即:c(NaHCO3)=2c(Na2CO3),综上所述选项A、B、D正确,选项C错误;答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碱金属元素单质的熔点随原子序数递增而降低
B. 同种元素的原子均有相同的质子数和中子数
C. 族序数等于其周期序数的元素一定是金属元素
D. ⅦA 族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用25%的稀H2SO4溶液与铁块反应制取氢气,下列措施能加快反应速率的是
A. 适当降低温度
B. 将铁块改为铁粉
C. 将所用硫酸改为98.3%浓硫酸
D. 滴加少量氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:(填序号,下同)
(1)A NH4Cl B KCl C H2S D F2 E NaOH F H2O2 G Na2O2
①属于共价化合物的是;___________
②只含有离子键的是;___________
③既含有离子键又含有共价键的是_____________
(2)在下列变化中,①I2升华,②烧碱熔化,③NaCl溶于水, ④HCl溶于水,⑤O2溶于水,⑥Na2O2溶于水,未发生化学键破坏的是____;仅发生离子键破坏的是___;仅发生共价键破坏的是____;既发生离子键破坏,又发生共价键破坏的是____。
(3)现有A:![]() 、
、![]() 、
、![]() ;B:H2、D2、T2;C:石墨、金刚石;D:
;B:H2、D2、T2;C:石墨、金刚石;D:![]() 、
、![]() 、
、![]()
四组微粒或物质,回答下列问题:①互为同位素的是_______(填字母序号,下同)。 ②互为同素异形体的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 电解精炼铜时,粗铜与直流电源的负极相连
B. 镀层破损后,镀锡铁片中铁比镀锌铁片中铁耐腐蚀
C. 常温时,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液pH=7
D. 合成氨反应N2(g) + 3H2(g)![]() 2NH3(g),当2v(N2)正 = v(NH3)逆时,反应达到平衡
2NH3(g),当2v(N2)正 = v(NH3)逆时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 氯化铝溶液与氨水反应:Al3++3OH-![]() Al(OH)3↓
Al(OH)3↓
B. 氧化镁与稀盐酸反应:MgO+2H+![]() Mg2++H2O
Mg2++H2O
C. 铜与氯化铁溶液反应:2Fe3++3Cu![]() 2Fe+3Cu2+
2Fe+3Cu2+
D. 稀硫酸与氢氧化钡溶液反应:SO42-+Ba2+![]() BaSO4↓
BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100 mL溶液,向溶液中加入下列物质,有关结论正确的是( )
加入物质 | 结论 | |
A | 50 mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO |
B | 0.05 mol CaO | 溶液中 |
C | 50 mL H2O | 由水电离出的c(H+)·c(OH-)不变 |
D | 0.1 mol NaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米CdSe(硒化镉)可用作光学材料。在一定条件下,由Na2SO3和Se(硒,与S为同族元素)反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒。流程图如下:
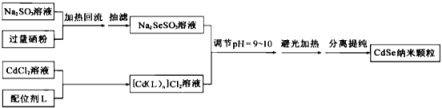
注:①CdCl2能与配位剂L形成配合物[Cd(L)n]Cl2
[Cd(L)n]Cl2=[Cd(L)n]2++2Cl-;[Cd(L)n]2+Cd2++nL
②纳米颗粒通常指平均粒径为1~100nm的粒子
请回答:
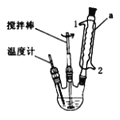
(1)下图加热回流装置中,仪器a的名称是______,进水口为_____(填1或2)
(2)研究表明,CdSe的生成分两步:①SeSO32-在碱性条件下生成HSe-;②HSe-与Cd2+反应生成CdSe。完成第①步反应的离子方程式 SeSO32-+_________=HSe-+__________。写出第②步反应的离子方程式_________________________________________。
(3)CdSe纳米颗粒的大小影响其发光性质。某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图2所示;同时探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图3所示。
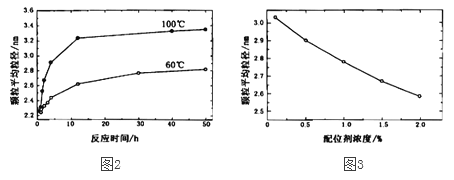
下列说法正确的是__________。
A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒
B.在图2所示的两种温度下,只有60℃反应条件下可得到2.7 nm的CdSe纳米颗粒
C.在其它条件不变时,若要得到较大的CdSe纳米颗粒,可采用降低温度的方法
D.若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com