
| A、(1)(2) |
| B、(1)(2)(3) |
| C、(1)(2)(3)(4) |
| D、(1)(2)(3)(4)(5) |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3保存在棕色试剂瓶里 |
| B、Li保存在煤油里 |
| C、用pH试纸测得某盐酸溶液的pH为2.3 |
| D、液溴保存在带橡胶塞的玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 除去HC1中含有的少量Cl2 |
B、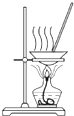 将硫酸铜溶液蒸干,制备蓝矾 |
C、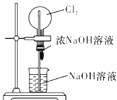 可以完成“喷泉”实验 |
D、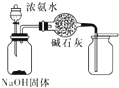 制取并收集干燥纯净的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在水中加KHCO3 |
| B、在水中加HCl |
| C、在水中加CuCl2 |
| D、将水加热至100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用锌粉代替锌粒 |
| B、改用更多的2mol/L硫酸溶液 |
| C、改用18mol/L硫酸溶液 |
| D、向该硫酸溶液中加入等体积的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蓝色 | B、黄色 | C、红色 | D、橙色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com