
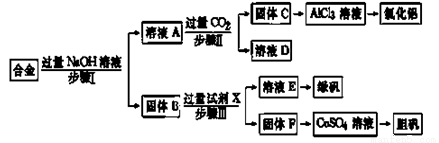
(12 分) 为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
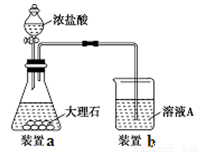
(3)进行步骤Ⅱ时,该小组用如图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:
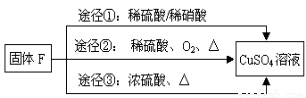
写出途径①中反应的离子方程式 , 请选出你认为的最佳途径并说明选择的理由 。
(1)2Al+2OH—+2H2O=2AlO2-+3H2↑(2分)
(2)稀硫酸或H2SO4(2分) 过滤(2分)
(3)在装置a、b之间增加一个盛有饱和NaHCO3溶液的洗气瓶(合理答案即给分)(2分)
(4)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O(2分)
途径②最佳,理由是原料利用率高,环境污染小(2分,结论1分,理由1分)
【解析】
试题分析:铝、铁和铜的合金中,只有金属铝可以和氢氧化钠溶液反应生成溶液A,偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体。
(1)步骤Ⅰ加过量的氢氧化钠,金属铝和氢氧化钠反应,金属铝溶解其中生成偏铝酸钠溶液,即2Al+2OH-+2H2O=2AlO2-+3H2↑。
(2)金属铁和金属铜不与氢氧化钠反应,金属铜和稀硫酸之间不反应,但是金属铁可以和稀硫酸之间反应生成硫酸亚铁和氢气,进而制的绿矾晶体,步骤Ⅰ、Ⅱ、Ⅲ均是固体和液体的分离操作,应该是过滤。
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个洗去氯化氢的装置,二氧化碳在饱和碳酸氢钠中不溶,氯化氢和碳酸氢钠反应生成二氧化碳气体,所以可在装置a、b之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢。
(4)金属铜可以和硝酸之间反应生成硝酸铜、一氧化氮和水,即3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所以途径②最佳。
考点:本题考查化学流程的分析、物质的分离和提纯、方程式的书写。


科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
下图各容器中盛有海水,铁在其中被腐蚀时由快到满的顺序是
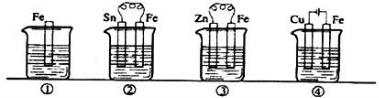
A、③>②>④>① B、②>①>③>④
C、④>②>③>① D、④>②>①>③
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列过程一定不能自发进行的是:
A.2N2O5(g)=4NO2(g)+O2(g);ΔH>0
B.2CO(g)=2C(s)+O2(g);ΔH>0
C.(NH4)2CO3(s)=NH4HCO3(s)+NH3(g);ΔH>0
D.2H2(g)+O2(g)=2H2O(l);ΔH<0
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.NH3·H2O NH4++OH-达到平衡后,升高温度平衡正向移动
NH4++OH-达到平衡后,升高温度平衡正向移动
B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率
C.明矾水解生成Al(OH)3胶体,可用作净水剂
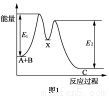
D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:填空题
(16分) 科学家发现在特殊条件下,水能表现出许多有趣的结构和性质。
(1)一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下。



水 热冰
采用“弱电场”的条件使水结成“热冰”,说明水分子是________分子(填“极性”或“非极性”)。请你展开想象,给“热冰”设计一个应用实例____________。
(2)用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。
① 释放出来的电子可以被若干水分子形成的“网”捕获而形成水合电子,你认为水分子间能形成“网”的原因是___________________。
② 由水分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式___ ________;该阳离子还能与水分子作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式_______。
(3)写出元素组成与水相同的物质W的电子式 , 写出W与FeCl2在酸性溶液中反应的离子方程式 。
(4)水溶液中存在H3O+ 离子,写出该微粒的结构式 (标出配位键)。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.反应CaCO3(s)=CaO(s)+CO2(g)在常温下不能发生,则该反应的△H>0
B.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中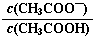 的值减小
的值减小
C.铅蓄电池在放电过程中,负极质量增加,正极质量减少
D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
下列各组物质之间通过一步就能实现如图所示转化的是
物质编号 | 物质转化关系 | a | b | c | d |
① |
| Na2O | Na2O2 | Na | NaOH |
② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
④ | NO | NO2 | N2 | HNO3 |
A.①②B.②③.C.②④D.①③
查看答案和解析>>
科目:高中化学 来源:2015届广东省韶关市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
(16分)某科研小组以难溶性钾长石(K2O·Al2O3·6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:
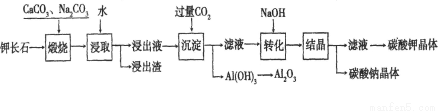
(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式: 。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式: 。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_____ ____。
Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_____ ____。
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示)_____ ____。
(4)上述工艺中可以循环利用的主要物质是____ ____、_____ ___和水。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com