
| A、电解MgCl2溶液可制金属镁 |
| B、可溶性铁盐或铝盐可用于水的净化 |
| C、在海轮外壳上装上锌块,可减缓船体的腐蚀速率 |
| D、“开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、该电池放电时,两极质量均增加 |
| B、放电时,正极的电极反应式为PbO2+4H++2e-═Pb2++2H2O |
| C、充电时,溶液中Pb2+向阳极移动 |
| D、充电时,阳极周围溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水稀释过程中,c(H+):c(OH-) 的值增大 | ||
| B、根据以上信息,可推断NH3?H2O为弱电解质 | ||
C、与pH=11.12的 NaOH溶液相比,NaOH溶液中c(Na+) 大于氨水中c(NH
| ||
| D、加入少量NH4Cl 固体,溶液中水的电离平衡:H2O?H++OH-正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 现象或事实 | 解释 |
A | 氢氟酸可用于蚀刻玻璃 | Si02是碱性氧化物 |
| B | 明矾可用作净水剂 | 明矾水解生成AI(OH)3沉淀 |
| C | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝的熔点高于铝的熔点 |
| D | 铁制容器用于储存、运输浓硝酸 | 铁制容器和浓硝酸不反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Kw |
| c(H+) |
| A、②③ | B、①③⑥ |
| C、①③⑤ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于0.2mol?L-1 |
| B、等于0.2mol?L-1 |
| C、小于0.2mol?L-1 |
| D、无法估算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

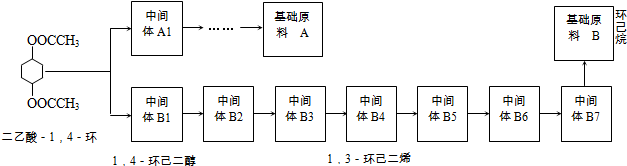
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Ba2+、Cl-、CO32- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、Na+、SO42-、Cl- |
| D、K+、Al3+、NO3-、I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com