
下列有关说法正确的是
A.放热反应在任何条件都能自发进行
B.应用盖斯定律,可计算某些难以直接测量的反应焓变
C.任何能使熵值增大的过程都能自发进行
D.△H>0,△S<0的化学反应一定能自发进行
科目:高中化学 来源: 题型:
下列关于碳氢化合物的说法正确的是( )
A.碳氢化合物的通式为CnH2n+2
B.燃烧产物为CO2和H2O的化合物一定是碳氢化合物
C.碳原子间以单键相连的烃是烷烃
D.烷烃分子的相对分子质量一定是偶数
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②碱性氧化物一定是金属氧化物
③根据丁达尔现象可将分散系分为胶体、溶液和浊液
④SiO2是酸性氧化物,能与NaOH溶液反应
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
A. ②③ B.②④⑤ C.①②④ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
关于某有机物  的性质叙述正确的是 ( )
的性质叙述正确的是 ( )
A、1 mol该有机物可以与3 mol Na发生反应、
B、1 mol该有机物可以与3 mol NaOH发生反应
C、1 mol该有机物可以与6 mol H2发生加成反应
D、1 mol该有机物分别与足量Na或NaHCO3反应,产生的气体在相同条件下体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备是:
I. 将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2,制得混有SiCl4杂质的TiCl4。
II. 将混有SiCl4杂质的TiCl4分离,得到纯净的TiCl4。
III. 在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O。
IV. TiO2·xH2O高温分解得到TiO2。
①TiCl4与SiCl4在常温下的状态是_______。II中所采取的操作名称_______。
|

②如实验IV中,应将TiO2.xH2O放在_______ (填仪器编号)中加热。
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a. O2→2O b. O+H2O→2OH(羟基) c. OH+OH→H2O2
①b中破坏的是 (填“极性共价键”或“非极性共价键”)。
②H2O2能清除路面空气中的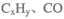 等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
(3)过氧化氢是重要的化学试剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量。
请填写下列空白:
①取10.00 mL密度为P g/mL的过氧化氢溶液稀释至250 mL。取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数配平及化学式填写在方框里。
 MnO+ H2O2+ H+= Mn2++ H2O+
MnO+ H2O2+ H+= Mn2++ H2O+
②滴定时,将高锰酸钾标准溶液注入______________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是____________________________。
③重复滴定三次,平均耗用C mol/L KMnO4标准溶液 V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________ (填“偏高”或“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各条件下发生反应X+Y=XY时,速率最快的是
A.常温下,20mL中含X、Y各0.003mol的溶液
B.常温下,100mL中含X、Y各0.005mol的溶液
C.常温下,0.1mol/L的X、Y溶液各l0mL相混合
D.标准状况下,0.1mol/L的X、Y溶液各l0mL相混合
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是( )
A.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则向含0.1 mol HCl的盐酸中加入4.0 gNaOH固体,放出热量等于5.73 kJ
B.等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),放出的能量相同
C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D.氢气的燃烧热为285.8 kJ·mol-1,则水分解的热化学方程式为:2H2O(l)=2H2(g) + O2(g) ΔH=+ 571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在a L的密闭容器里,于一定温度下进行2A(g)+B(g)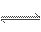 2C(g)的可逆反应。容器内开始加入下列各组物质,在达到平衡时逆反应速率最大的一组物质是( )]
2C(g)的可逆反应。容器内开始加入下列各组物质,在达到平衡时逆反应速率最大的一组物质是( )]
A.2 mol A和1 mol B B.1 mol A和1 mol B
C.1 mol A和2 mol B D.1 mol B和1 mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H—H,H—O,和O==O键的键能分别为436KJ.mol-1,463 KJ.mol-1,495 KJ.mol-1,下列热化学方程式正确的是( )
A.H2O(g)==H2(g)+1/2O2(g) △H =-485 KJ.mol-1
B.H2O(g)==H2(g)+1/2O2(g) △H = + 485 KJ.mol-1
C.2 H2(g) + O2(g)==2 H2O(g) △H = + 485 KJ.mol-1
D.2 H2(g) + O2(g)==2 H2O(g) △H =-485 KJ.mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com