
| A. | 己烷(己烯) 溴水 分液 | B. | 淀粉溶液(NaCl) 水 过滤 | ||
| C. | CH3CH2OH(CH3COOH) CaO 蒸馏 | D. | CO2(SO2) Na2CO3溶液 洗气 |
分析 A.己烯与溴水反应,但溴易溶于己烷;
B.溶液与胶体均可透过滤纸;
C.乙酸与CaO反应后,增大与乙醇的沸点差异;
D.二者均与碳酸钠溶液反应.
解答 解:A.己烯与溴水反应,但溴易溶于己烷,不能除杂,应蒸馏分离,故A错误;
B.溶液与胶体均可透过滤纸,不能分离,应选渗析法,故B错误;
C.乙酸与CaO反应后,增大与乙醇的沸点差异,然后蒸馏可分离,故C正确;
D.二者均与碳酸钠溶液反应,不能除杂,应选饱和碳酸氢钠溶液、洗气,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,注意有机物的性质应用,题目难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:解答题
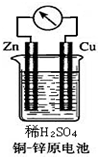 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
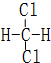 和
和 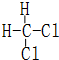 同一种物质.
同一种物质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是银白色的柔软金属,密度都比水小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 单质的熔沸点随着原子序数的增加而升高 | |
| D. | 碱金属单质与水剧烈反应生成碱和氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 114号元素衰变成112号元素是化学变化 | |
| B. | 114号元素位于第12列 | |
| C. | ${\;}_{114}^{263}$X的中子数与质子数之差为149 | |
| D. | 112号元素位于周期表第七周期第ⅡB族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若HnXOm为强酸,则Y是活泼的非金属元素 | |
| C. | 若Y的最低化合价是-2,则Z的最高正价为+6 | |
| D. | 若X的最高正价为+5,则五种元素都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 暖冰中水分子是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 暖冰中水分子的各原子均满足8电子稳定结构 | |
| C. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:PH3<NH3<H2O | B. | 碱性:Ba(OH)2<Ca(OH)2<KOH | ||
| C. | 熔点:MgBr2<SiCl4<BN | D. | 酸性:H2CO3<HClO<HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com