
已知蓄电池在放电时起原电池的作用,在充电时起电解池的作用。汽车上用的铅蓄电池是以一组充满海绵状灰铅的铅板和另一组结构相似的充满二氧化铅的铅板组成。两个电极用稀硫酸作电解质溶液。在放电时,两极发生的反应可分别表示为:
Pb+S-2e- PbSO4
PbSO4
PbO2+4H++S+2e- PbSO4+2H2O
PbSO4+2H2O
充电时,两极发生的反应分别表示为:
PbSO4+2e- Pb+S
Pb+S
PbSO4+2H2O-2e- PbO2+4H++S
PbO2+4H++S
在蓄电池生产和使用时,下列说法中正确的是( )
| A.生产和使用铅蓄电池,不会造成环境污染 |
| B.生产和使用铅蓄电池时,可能引起铅中毒和环境污染 |
| C.使用铅蓄电池时,若铅板上有1 mol铅反应就消耗1 mol H2SO4 |
| D.在使用时,电池内溶液的密度会增大 |
科目:高中化学 来源: 题型:单选题
早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融) 4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
| A.电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na |
| B.盖·吕萨克法制钠原理是嫡的增加带动了反应的进行 |
| C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1 |
| D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下图,下列判断中正确的是
| A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
| B.烧杯b中发生反应为2Zn-4eˉ =2Zn2+ |
| C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极 |
| D.烧杯a中发生反应O2 + 4H++ 4eˉ = 2H2O,溶液pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
体积为1 L的某溶液中含有的离子如表所示:
| 离子 | Cu2+ | Al3+ |  | Cl- |
| | 1 | 1 | a | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O CH3COOH+4H+。下列有关说法正确的是( )
CH3COOH+4H+。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4 mol电子转移,则在标准状况下消耗4. 48 L氧气 |
C.电池反应的化学方程式为:CH3CH2OH+O2 CH3COOH+H2O CH3COOH+H2O |
D.正极上发生的反应为:O2+4e-+2H2O 4OH- 4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是( )
| A.①③②④ | B.①③④② |
| C.③④②① | D.③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。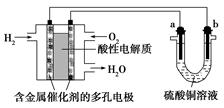
| A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将两金属A、B分别用导线相连接,并同时插入电解质溶液中,发现A极的质量增加,则下列说法正确的是( )
A.金属活动性:A>B
B.A极是正极,电解质溶液可以是盐酸
C.B极是负极
D.要判断A极与B极是正极还是负极,还需考虑电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO2-+H2O。下列说法不正确的是( )
| A.该电池的优点是电极材料和电解质用完后可以更换 |
| B.该电池发生氧化反应的是金属铝 |
| C.电极的正极反应式为3ClO-+3H2O+6e-=3Cl-+6OH- |
| D.当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com