
【题目】下列说法中,正确的是( )
A.硅元素在自然界里均以化合态存在B.SiO2硬度大,可用于制造光导纤维
C.NH3易溶于水,可用作制冷剂D.粗硅制备时,发生的反应为C+SiO2= Si +CO2↑
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 任何条件下,化学反应的焓变都等于化学反应的反应热
B. 需要加热才能进行的反应一定是吸热反应
C. 物质具有的能量越高,物质的稳定性越强
D. 在确定的化学反应体系中,反应物的总能量与生成物的总能量一定不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃与溴化氢、水加成时,产物有主次之分,例如:
![]()

下列框图中B、C、D都是相关反应中的主要产物(部分条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、1种氢原子。

上述框图中,B的结构简式为________;属于取代反应的有__________(填框图中序号),属于消去反应的有__________(填序号);写出反应④的化学方程式(只写主要产物,标明反应条件):__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL 0.1mol/L的盐酸中逐滴加入0.2mol/L的氨水,溶液的pH与所加氨水的体积关系如图所示,下列说法正确的是

A. a、b、c三点比较,水的电离程度a点最大
B. 在c点:c(NH4+)+c(NH3·H2O)= 0.2mol/L
C. 在a点:c(OH-)<c(H+)<c(NH4+)<c(NH3·H2O)<c(Cl-)
D. 在b点,盐酸与氨水恰好完全中和, c(NH4+)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.酸性氧化物:SO2、SO3、CO2、CO
B.碱:烧碱、纯碱、苛性钾、氢氧化钡
C.混合物:铝热剂、漂白粉、水煤气、氢氧化铁胶体
D.电解质:稀硫酸、氢氧化钠、氯化钠、MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2与CH4的反应使之转化为CO 和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知该转化反应为CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH,则加快该反应的化学反应速率,应采用的有效措施有___________________________(填写两种)。
2CO(g)+2H2(g) ΔH,则加快该反应的化学反应速率,应采用的有效措施有___________________________(填写两种)。
(2)在密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH,测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g) ΔH,测得CH4的平衡转化率与温度、压强的关系如下图所示。

①由图可知,该反应的ΔH_____0 (填写“大于”或者“小于”),P1、P2、P3、P4由大到小的顺序为_________________________。
②工业生产时一般会选用P4和1250℃进行合成,请解释其原因______________________________。
③在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为_________________mol·L-1·min-1。
④该温度下,反应的平衡常数K的数学表达式为K=_______,经计算K的数值为K=_____________(保留3位有效数字),若要使K减小可采取的措施是_________________。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g) ![]() CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。
① 在恒温恒容下,如果从反应物出发建立平衡,可认定已达平衡状态的是_______________
A. H2、CO和H2O的物质的量之比为1:1:1 B.体系压强不再变化
C. 气体平均相对分子质量不变 D.混合气体的密度保持不变
② 在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向_______(填“正”或“逆”)反应方向移动,达到新的平衡后,气体的平均摩尔质量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生小红利用右下图装置合成乙酸乙酯的步骤如下:在圆底烧瓶A 内加入乙醇,浓硫酸和乙酸,瓶口竖直安装仪器B,加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:

(1)仪器B的名称为_____,冷凝水的流入方向是_______________(填“a”或“b”)。
(2)在烧瓶中放入碎瓷片,其作用是___________________;如果加热一段时间后发现忘记添加碎瓷片,应该采取的正确操作是___________(填字母)。
A.冷却后补加 B.立即补加 C.不需补加 D.重新配料后加入
(3)反应中加入过量乙醇,其目的是___________________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是______________;浓硫酸用量又不能过多,原因是________________________。
(4)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是__________________________________。
(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯。他们分别将粗产品与一定量NaOH溶液混合后,蒸馏收集76℃~78℃的产品(已知:乙醇的沸点78℃,乙酸的沸点117.9℃,乙酸乙酯的沸点77℃)。实验结果:甲得到溶于水的液体X;乙得到难溶于水。但显酸性的液体Y;则:①X主要含_________________________。②Y主要_________________________。__________________________。
(6)丙同学重新设计了提纯粗产品的方案,流程如下:

由此回答下列问题:
①试剂a是:_______________ ,其作用是溶解乙醇、反应消耗乙酸和____________________。
②分离方法[Ⅰ]是_____________,试剂b是___________,分离方法[Ⅱ]是_____________。
(7)用30g乙酸与46g乙醇反应,产率为67%,则制得的乙酸乙酯的质量为__________g(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如右图所示。以下有关该物质的说法中正确的是( )
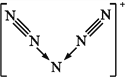
A. 每个N5+中含有35个质子和36个电子
B. 该离子中有非极性键和配位键
C. 该离子中含有2个π键
D. 与PCl4+互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修5:有机化学基础】
有机物G是一种医药中间体,可通过如图所示路线合成。A是石油化工的重要产品且分子中所有原子在同一平面上,H为碳氢化合物。
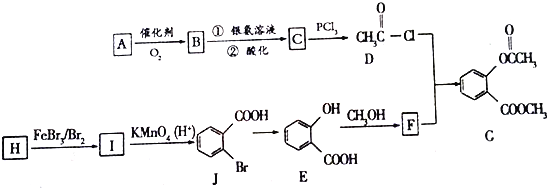
已知: 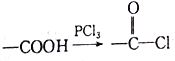
请回答以下问题:
(1)A的结构简式是________。
(2)H→I的化学反应方程式为________,B与银氨溶液反应的化学方程式是________ 。
(3)C→D的反应类型是________,I→J的反应类型是________ 。
(4)E→F的反应条件是________ 。
(5)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是________ 。
(6)满足以下条件的F的同分异构体(含F)共有________种(填数字)。
①能与氯化铁溶液发生显色反应
②红外光谱等方法检测分子中有![]() 结构
结构
③苯环上有两个取代基
其中能与碳酸氢钠溶液反应且核磁共振氢谱测定有5个吸收峰的同分异构体的结构简式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com