
| A. | 过氧化钠放置在空气中,最终转变为白色粉末Na2CO3 | |
| B. | Ca(ClO)2溶液通入CO2,溶液变浑浊;再加入品红溶液,红色褪去 | |
| C. | 打磨过的铝箔和未打磨的铝箔分别在空气中灼烧,两种铝箔均熔化但不滴落,说明氧化铝熔点比铝高 | |
| D. | 在一定条件下,金属Na、Mg、Fe与水反应都生成H2和对应的碱 |
分析 A.过氧化钠可与空气中二氧化碳反应;
B.次氯酸钙溶液通入二氧化碳生成具有漂白性的次氯酸;
C.氧化铝熔点较高,难以熔化;
D.铁和水反应生成Fe3O4.
解答 解:A.过氧化钠可与空气中二氧化碳反应,最终产物为碳酸钠,故A正确;
B.次氯酸钙溶液通入二氧化碳生成具有漂白性的次氯酸,可使品红褪色,故B正确;
C.氧化铝熔点较高,难以熔化,则打磨过的铝箔和未打磨的铝箔分别在空气中灼烧,在表面生成氧化铝膜,两种铝箔均熔化但不滴落,故C正确;
D.Na、Mg均满足要求,而Fe与H2O(g)反应生成Fe3O4和H2,得不到碱,故D错误;
故选D.
点评 本题考查较为综合,为高频考点,侧重于物质的性质与应用的考查,题目难度不大,注意相关基础知识的积累.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:99 | B. | 1:100 | C. | 100:1 | D. | 99:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁 | B. | 铁和铜 | C. | 铁和银 | D. | 铁、铜、银 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
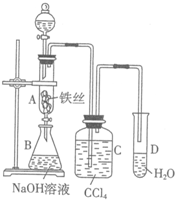 某化学课外小组用图装置制取溴苯.
某化学课外小组用图装置制取溴苯. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验①中产生的气体为氨,并可得原溶液中c(NH4+)=0.1 mol•L-1 | |
| B. | 实验③中的沉淀里一定有BaSO4,可能有Mg(OH)2 | |
| C. | 若要确定原溶液中是否含有Cl-,无需另外再设计实验验证 | |
| D. | 原溶液中一定含有Na+,且c(Na+)≥0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
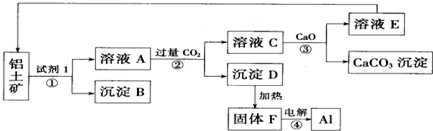
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com