
 A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;D、E、F同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答问题:
A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;D、E、F同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答问题:分析 在前四周期中原子序数依次增大的六种元素A、B、C、D、E、F、G中,A的原子核外电子只有一种运动状态,故A为H;周期元素B、C的价电子层中未成对电子数都是2,则B、C核外电子排布为1s22s22p2或1s22s22p4,分别为C、O;E核外的s、p能级的电子总数相等,则E为Mg;F原子序数大于E,F与E同周期且第一电离能比E小,则F为Al;D、E、F同周期,则D为Na元素;G的+1价离子(G+)的各层电子全充满,元素的基态原子最外能层只有一个电子,其它能层均已充满电子,则核外电子数为2+8+18+1=29,故G为Cu,据此进行解答.
解答 解:在前四周期中原子序数依次增大的六种元素A、B、C、D、E、F、G中,A的原子核外电子只有一种运动状态,故A为H;周期元素B、C的价电子层中未成对电子数都是2,则B、C核外电子排布为1s22s22p2或1s22s22p4,分别为C、O;E核外的s、p能级的电子总数相等,则E为Mg;F原子序数大于E,F与E同周期且第一电离能比E小,则F为Al;D、E、F同周期,则D为Na元素;G的+1价离子(G+)的各层电子全充满,元素的基态原子最外能层只有一个电子,其它能层均已充满电子,则核外电子数为2+8+18+1=29,故G为Cu,
(1)E为Mg元素,其原子核外有12个电子,根据构造原理书写其核外电子排布式为1s22s22p63s2,
故答案为:1s22s22p63s2;
(2)D为Na元素,钠盐的焰色反应的火焰呈黄色;许多金属盐都可以发生焰色反应,其原因为:灼烧时电子从基态到激发态,激发态电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长光的形式释放能量,从而出现不同的颜色,
故答案为:黄;激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长(可见光区域)光的形式释放能量;
(3)由元素H、C、Al组成的原子个数比9:3:1的一种物质,分子中含三个相同的原子团,其结构简式为Al(CH3)3,该物质遇水爆炸,生成白色沉淀和无色气体,反应的化学方程式为:Al(CH3)3+3H2O=Al(OH)3↓+3CH4↑,
故答案为:Al(CH3)3;Al(CH3)3+3H2O=Al(OH)3↓+3CH4↑;
(4)GC和G2C分别为CuO、Cu2O,由于Cu2+离子外围电子排布式为3d9,而Cu+离子外围电子排布式为3d10,为全满稳定状态,所以Cu2O比CuO稳定,
故答案为:Cu2+离子外围电子排布式为3d9,而Cu+离子外围电子排布式为3d10,为全满稳定状态,所以Cu2O比CuO稳定;
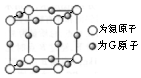
(5)晶胞中Cu原子数目=12×$\frac{1}{4}$=3、N原子数目=8×$\frac{1}{8}$=1,故该化合物的化学式为:Cu3N;
以顶点N原子为例,每个N原子周围距离最近的铜原子有6个,所以N的配位数为6;
设G原子与氮原子最近的距离为bcm,则晶胞棱长=2bcm,则晶胞体积=(2bcm)3,故晶体的密度=$\frac{\frac{M}{{N}_{A}}}{V}$=$\frac{\frac{206}{{N}_{A}}}{(2b)^{3}}$g•cm-3=ag•cm-3,则b=$\root{3}{\frac{206}{8a{N}_{A}}}$cm=$\root{3}{\frac{206}{8a{N}_{A}}}$×1010pm,
故答案为:Cu3N;6;$\root{3}{\frac{206}{8a{N}_{A}}}$×1010.
点评 本题考查位置、结构与性质关系的综合应用,为高频考点,题目难度较大,涉及元素推断、晶胞计算、原子核外电子排布等知识,明确物质结构、原子结构及基本原理是解本题关键,难点是晶胞计算,试题培养了学生的分析、理解能力及逻辑推理能力.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
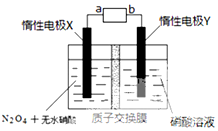 汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染.
汽车尾气排放的NO和CO都是有毒的气体,科学家正在研究利用催化技术将尾气中的NO和CO转变成无毒的CO2和N2,减少污染.| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-4mol/L | 3.00 | 2.25 | 1.75 | 1.36 | 1.00 | 1.00 |
| c(CO)/×10-4mol/L | 4.00 | 3.25 | 2.75 | 2.36 | 2.00 | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在100℃、101 kPa条件下,液态水的汽化热为40.69 kJ•mol-1,则H2O(g)?H2O(l)△H=40.69 kJ•mol-1 | |||||||||||
| B. | 已知:
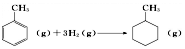 的焓变为△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]kJ•mol-1=-384 kJ•mol-1 的焓变为△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]kJ•mol-1=-384 kJ•mol-1 | |||||||||||
| C. | 在一定条件下,某可逆反应的△H=+100kJ•mol-1,则该反应正反应活化能比逆反应活化能大100kJ•mol-1 | |||||||||||
| D. | 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 400mL 2mol/L HCl | B. | 300mL 2mol/L H2SO4 | ||
| C. | 100mL 3mol/L HNO3 | D. | 500mL 18.4mol/L H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 |
| 取2mL上述FeSO4溶液于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡.测得反应后溶液pH=0.9 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
| 操作 | 现象 |
| 取2mL 5% H2O2溶液于试管中,加入5滴上述FeSO4溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊.测得反应后溶液pH=1.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol白磷中含共价键数均为4NA | |
| B. | 1 mol-CH3中含有的电子数为9 NA | |
| C. | 1 mol Na2O2 固体中含离子总数为4 NA | |
| D. | 标准状况下,2.24 L SO3所含分子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 证明某红棕色气体是溴蒸气还是NO2,可用AgNO3溶液检验,观察是否有沉淀生成 | |
| B. | 将点燃的镁条迅速投入到集满CO2的集气瓶中,观察到镁条在集气瓶底部继续燃烧 | |
| C. | 实验室用氢氧化钠标准溶液滴定未知浓度的醋酸溶液时,选用甲基橙做指示剂 | |
| D. | 向盛有5mL苯酚溶液的试管中滴入2~3滴稀溴水,边加边振荡,立即观察到有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com