
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
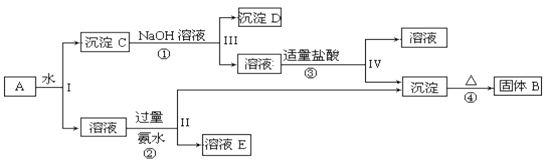
据此回答下列问题:
(1)I、II、III、IV四步操作采取的分离方法是___________________。
(2)根据上述框图反应关系,写出下列B、C、E所含物质的化学式沉淀固体B________________;C______________________;E_______________
(3)写出①、②、④三个反应方程式(有离子反应的写离子方程式,没有的写化学方程式)
①____________________________ ② ____________________________
④__________________________
【答案】过滤 Al2O3 Al2O3、Fe2O3 K2SO4、(NH4)2SO4 Al2O3+2OH- = 2AlO2- + H2O Al3+ +3NH3·H2O=Al(OH)3↓+3NH4+ 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】
混合物A加水后,![]() 和
和![]() 均不溶于水,变成沉淀C,溶液中为
均不溶于水,变成沉淀C,溶液中为![]() ,KAl(SO4)2溶液中加入过量氨水后铝离子会转变成
,KAl(SO4)2溶液中加入过量氨水后铝离子会转变成![]() ,溶液中含
,溶液中含![]() 和
和![]() 、过量氨水,即溶液E。向沉淀C即
、过量氨水,即溶液E。向沉淀C即![]() 和
和![]() 中加入NaOH溶液,只有
中加入NaOH溶液,只有![]() 会溶于NaOH变成
会溶于NaOH变成![]() ,沉淀D为不溶的
,沉淀D为不溶的![]() ;向
;向![]() 溶液中加入适量盐酸可以得到
溶液中加入适量盐酸可以得到![]() 沉淀和
沉淀和![]() 溶液,最后加热
溶液,最后加热![]() 分解得到
分解得到![]() ,即固体B,据此分析作答。
,即固体B,据此分析作答。
(1)步骤I、II、III、IV均为分离不溶性沉淀和溶液,因此选用的方法为过滤;
(2)根据前面的分析,B为![]() ,C为
,C为![]() 和
和![]() 二者混合物,E为
二者混合物,E为![]() 和
和![]() 混合物;
混合物;
(3)根据题图和前面的分析来写即可:①为![]() ;②为
;②为![]() ,注意氨水不能拆;④为
,注意氨水不能拆;④为![]() ,该过程无离子反应方程式。
,该过程无离子反应方程式。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】在紫外线的作用下,氧气可生成臭氧:3O2![]() 2O3,一定条件下该反应达到平衡状态的标志是( )
2O3,一定条件下该反应达到平衡状态的标志是( )
A. 单位时间内生成2 mol O3,同时消耗3 mol O2
B. O2的消耗速率0.3 mol·L-1·s-1,O3的消耗速率0.2 mol·L-1·s-1
C. 容器内,2种气体O3、O2浓度相等
D. 气体密度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A. NH3![]() NO2
NO2![]() HNO3B. Al
HNO3B. Al![]() NaAlO2(aq)
NaAlO2(aq)![]() NaAlO2(s)
NaAlO2(s)
C. Fe![]() Fe2O3
Fe2O3![]() FeD. AgNO3(aq)
FeD. AgNO3(aq)![]() [Ag(NH3)2OH(aq)]
[Ag(NH3)2OH(aq)]![]() Ag
Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量的铜和含有2.4×10-3mol硝酸的某浓硝酸完全反应,共收集到标准状况下气体体积22.4 mL。参加反应的铜的质量是( )
A. 38.4×10-3gB. 44.8×10-3gC. 48.3×10-3gD. 57.6×10-3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水约占地球表面积的71%,具有十分巨大的开发潜力。下图是开水资源综合利用的工艺图,以下说法正确( )

A. 电解NaCl溶液时可用铁做电极,其离子方程式为:2Cl- + 2H2O = 2OH-+ H2↑+ Cl2↑
B. 向苦卤中加入Cl2的作用是置换出溴单质,该过程体现了还原性:Cl- > Br-
C. 实验室模拟海水提取淡水,除夹持装置外只用到的仪器有蒸馏烧瓶、酒精灯、锥形瓶
D. Br2 与SO2的水溶液发生反应的离子方程式为:Br2 + SO2 + 2H2O =4H+ + 2Br- + SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。下图为铁元素的价类二维图,其中的箭头 表示部分物质间的转化关系,下列说法正确的是( )
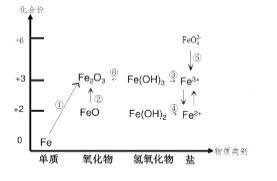
A. 铁与高温水蒸气的反应可实现上述转化①
B. FeO 是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末
C. 由图可预测:高铁酸盐( FeO42- )具有强氧化性,可用于消毒。FeO42- 与水反应最终可生成 Fe(OH)3胶体,从而吸附水中的悬浮物,故高铁酸盐可用做净水剂
D. 加热 Fe(OH)3 发生转化⑥,加水溶解可实现转化③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铋酸钠(NaBiNO3)检验溶液中的Mn2+,反应方程式为:4MnSO4+10NaBiO3+14H2SO4═4NaMnO4+5Bi2(SO4)3+3Na2SO4+口,下列说法不正确的是
A. 口内的物质为水,配平系数为14。
B. 若生成1mol NaMnO4,则转移5mole-
C. 反应方程式中的硫酸可换为盐酸
D. 溶液中有Mn2+的现象是溶液变为紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出这四种元素的元素符号:T_______;X_______;Y_______;Z_______。
(2)写出元素T的原子结构示意图_____________________________
(3)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是__________(填序号)。
①Y单质的熔点比Z单质低 ②Y的化合价比Z低
③Y单质与水反应比Z单质剧烈 ④Y最高价氧化物的水化物的碱性比Z强
(4)X元素的气态氢化物与其最高价含氧酸反应的方程式为______________________
(5)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉的主要成分是次氯酸钙和氯化钙。请回答下列问题:
(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式(若涉及氧化还原反应,请标注电子转移情况):____________________________。
(2)某化学小组将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,共收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为_____________(假设漂白粉中的其它成份不与硝酸反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com