
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2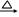 2PCl3;2P+5Cl2(过量) 2PCl3;2P+5Cl2(过量)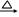 2PCl5 2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
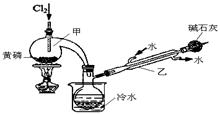
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI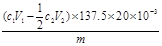
 H3PO4+2HI,然后加入(NH4)3BO3溶液,与HI和H3PO4反应生成H3BO3,最后利用Na2S2O3溶液滴定为反应的I2,根据消耗的I2,计算PCl3的质量,进而确定样品中PCl3的质量分数;①、步骤3:准确加入c1mol?L-1碘溶液V1 mL(过量),再迅速加入足量(NH4)3BO3溶液;②滴定剩余的I2消耗Na2S2O3物质的量为c2V2×10-3mol,由I2+2Na2S2O3=Na2S4O6+2NaI剩余的I2为1/2c2V2×10-3mol,所以与H3PO3反应的I2为(c1V1×10-3-1/2c2V2×10-3) mol,根据关系式PCl3~H3PO3~I2可知,mg产品中PCl3的质量为(c1V1×10-3-1/2c2V2×10-3)×20×137.5g; PCl3的质量分数为
H3PO4+2HI,然后加入(NH4)3BO3溶液,与HI和H3PO4反应生成H3BO3,最后利用Na2S2O3溶液滴定为反应的I2,根据消耗的I2,计算PCl3的质量,进而确定样品中PCl3的质量分数;①、步骤3:准确加入c1mol?L-1碘溶液V1 mL(过量),再迅速加入足量(NH4)3BO3溶液;②滴定剩余的I2消耗Na2S2O3物质的量为c2V2×10-3mol,由I2+2Na2S2O3=Na2S4O6+2NaI剩余的I2为1/2c2V2×10-3mol,所以与H3PO3反应的I2为(c1V1×10-3-1/2c2V2×10-3) mol,根据关系式PCl3~H3PO3~I2可知,mg产品中PCl3的质量为(c1V1×10-3-1/2c2V2×10-3)×20×137.5g; PCl3的质量分数为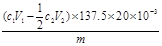 。
。

科目:高中化学 来源:不详 题型:单选题
| A.约为5mL | B.大于25 mL | C.等于25 mL | D.小于25 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②④ | C.①③ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
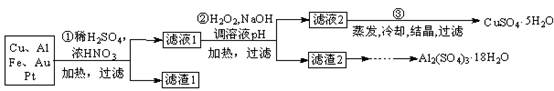

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.进行焰色反应时,必须用稀盐酸洗涤并灼烧铂丝,然后再进行实验 |
| B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| C.读取滴定管内液体体积时,俯视读数导致读数偏大 |
| D.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用广泛pH试纸测得氯水的pH为2.1 |
| B.用50mL量筒量取23.00 mL浓盐酸 |
| C.用温度计测量出酒精的沸点为78.5℃ |
| D.用托盘天平称量氧化铜粉末为11.70g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用待测液润洗滴定用的锥形瓶 |
| B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 |
| C.用稀硝酸酸洗涤盛做过银镜反应的试管 |
| D.液溴保存时液面覆盖一层水,装在带橡胶塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

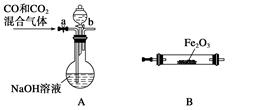

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com