
| A.用酸性KMnO4溶液鉴别乙烯和乙炔 |
| B.将铁屑、溴水、苯混合制溴苯 |
| C.在苯和硝基苯采用分液的方法分离 |
| D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:实验题
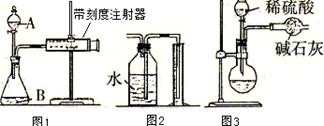
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ①测定上述实验用的Fe(NO3)3溶液的pH值 | |
| ② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2CrO42-+2H+左移,导致滴定终点滞后。
2CrO42-+2H+左移,导致滴定终点滞后。| 实验序号 | FeSO4溶液的体积读数/mL | |
| 滴定前 | 滴定后 | |
| 1 | 0.10 | 16.20 |
| 2 | 0.30 | 15.31 |
| 3 | 0.20 | 15.19 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
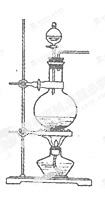
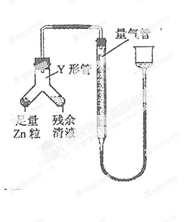
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
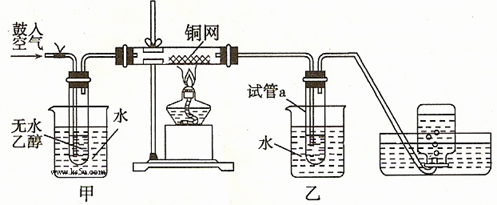
 。(填写化学式或分子式)
。(填写化学式或分子式) 查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 装置 | 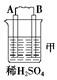 | 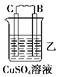 | 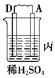 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙烷和氯气光照下制取纯净的氯乙烷 | B.用分液漏斗分离环己烷和水的混合液体 |
| C.用浓氨水洗涤做过银镜反应的试管 | D.在苯和溴水的混合物中加入铁粉制取溴苯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 NaCl杂质,为测
NaCl杂质,为测 定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。
定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。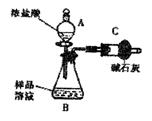
 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)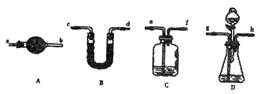
选用的 仪器 仪器 | | | | | |
| 添加的药品及必要的操作 | | | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com