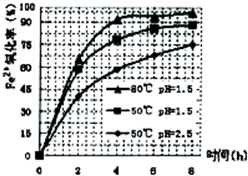
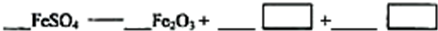(2010?茂名二模)化学兴趣小组发现,往CuSO
4溶液中加入一定浓度的Na
2CO
3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀.为此,小组同学对沉淀成份作了如下探究:
I.探究蓝色沉淀的成份
[猜想]:蓝色沉淀①可能是CuCO
3;②可能是Cu(OH)
2;③是两者的混合物.
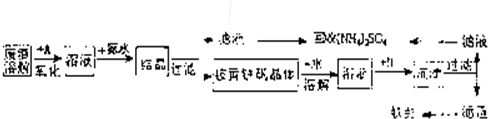
[设计方案]:小组同学利用下列装置通过实验测定其组成
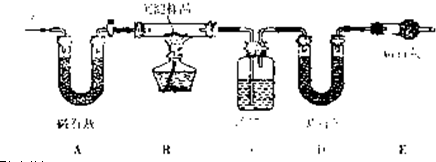
[问题与讨论]
(1)写出②猜想的依据
CO2-2水解成碱性,Cu2+与OH-结合生成Cu(OH)2
CO2-2水解成碱性,Cu2+与OH-结合生成Cu(OH)2
.
(2)装置A中碱石灰的作用是
吸收空气中的H2蒸汽和CO2
吸收空气中的H2蒸汽和CO2
.
(3)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是
通过量的空气并称量C、D的质量
通过量的空气并称量C、D的质量
.
(4)若沉淀样品的质量为mg.装置C质量增加了ng,则沉淀中CuCO
2的质量分数为
[1-(49n/9m)]
[1-(49n/9m)]
.
II.通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式为CUSO
4?3Cu(OH)
2).请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法
将浊液过滤,并把沉淀用蒸馏水洗涤至洗涤液用BaCl2溶液检验不出SO42-后,加入足量稀盐酸溶解浅绿色沉淀,再用BaCl2溶液检验,若溶液中有大量白色沉淀生成,则浅绿色没淀中有SO42-
将浊液过滤,并把沉淀用蒸馏水洗涤至洗涤液用BaCl2溶液检验不出SO42-后,加入足量稀盐酸溶解浅绿色沉淀,再用BaCl2溶液检验,若溶液中有大量白色沉淀生成,则浅绿色没淀中有SO42-
.