
科目: 来源: 题型:选择题
| A. | 滴定过程中,高锰酸钾被氧化,草酸钠被还原 | |
| B. | 用酸式滴定管量取草酸钠溶液 | |
| C. | 该反应中,消耗的草酸钠与高锰酸钾的物质的量之比为5:2 | |
| D. | 为便于滴定终点的判断,滴定时必须往体系中加入指示剂 |
查看答案和解析>>
科目: 来源: 题型:解答题



查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ①⑤ | C. | ①③④⑤ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A |
 ;
; ;
;查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 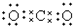 | B. | K+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H]- | ||
| C. | 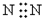 | D. |  |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaOH、Mg(OH)2、H3PO4、H2SO4 | B. | NaOH、KOH、H2SO4、HClO4 | ||
| C. | Be(OH)2、Ca(OH)2、HBrO4、HClO4 | D. | Mg(OH)2、Ba(OH)2、H3PO4、H2SO4 |
查看答案和解析>>
科目: 来源: 题型:解答题
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:解答题
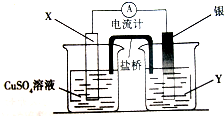 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
| 弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 | 1.8×l0-5 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com