
科目: 来源: 题型:解答题
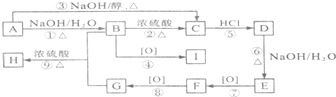
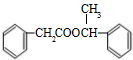 .
. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl.
+NaCl.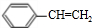 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$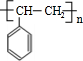 .
.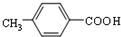 .
.查看答案和解析>>
科目: 来源: 题型:解答题
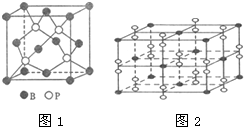 As、N、0等非金属元素的化合物在工业生产中有重要的应用.
As、N、0等非金属元素的化合物在工业生产中有重要的应用.查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
| Ksp(单位略) | 1.1×10-11 | 2.3×10-3 | 1.8×10-10 | 1.9×10-12 |
| A. | 浓度均为0.2 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 | |
| B. | 将O.001 mol•L-1的AgN03溶液滴入O.001 mol•L-1的KCl和O.001 mol•L-1 的K2CrO4混合溶液中.先产生Ag2Cr04沉淀 | |
| C. | 0.ll mol•L-1的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 | |
| D. | 在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
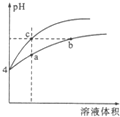 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是( )| A. | a、b、c三点溶液的Kw相同 | |
| B. | b点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| C. | 用等浓度的NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb>Vc | |
| D. | a、b、c三点溶液中水的电离程度a>b>c |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 灼热铜丝发生的现象变化为紫红色与黑色交替出现,甲醇发生还原反应 | |
| B. | C中有机产物易溶于水,与水分子间只形成1种氢键 | |
| C. | 检验C中产物的试剂可用1 mol•L-1的CuS04溶液2 mL和O.4 mol•L-1的NaOH溶液4 mL混合得到 | |
| D. | 可用酸性高锰酸钾溶液检验产物生成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | “雨后彩虹”是一种与光学和胶体性质相关的自然现象 | |
| B. | 纯银器表面在空气渐渐变暗,是电化学腐蚀所致 | |
| C. | 右图电流表指针偏转,有电流通过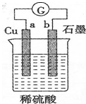 | |
| D. | 在食品中科学使用食品添加剂对人体无害 |
查看答案和解析>>
科目: 来源: 题型:选择题
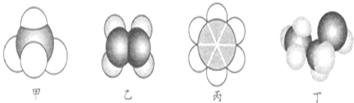
| A. | 22.4 L甲中含有10 mol电子 | |
| B. | 乙与乙的加聚产物都能使溴水褪色 | |
| C. | 丙不能与溴水、酸性高锰酸钾溶液发生反应 | |
| D. | 丙、丁都可以萃取溴水中的溴单质 |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.
查看答案和解析>>
科目: 来源: 题型:解答题
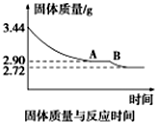 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题

 NaClO+H2↑.电解结束后一段时间,有同学发现铁电极表面变成红褐色,则反应方程式为3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
NaClO+H2↑.电解结束后一段时间,有同学发现铁电极表面变成红褐色,则反应方程式为3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com