
科目: 来源: 题型:解答题
 在元素周期表前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.
在元素周期表前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子. ; A2D由液态形成晶体时密度减小,其主要原因水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小(用文字叙述).
; A2D由液态形成晶体时密度减小,其主要原因水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小(用文字叙述).查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
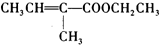 ;以化合物A为原料合成F的工艺流程如图:
;以化合物A为原料合成F的工艺流程如图:

 .
.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHCO3溶液加水稀释,$\frac{c(N{a}^{+})}{c(HC{{O}_{3}}^{-})}$的比值保持增大 | |
| B. | 在0.1 mol•L一1氨水中滴加0.lmol•L一1盐酸,恰好完全中和时溶液的pH<7 | |
| C. | 向0.lmol/L Na2S03溶液中加人少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| D. | 0.lmol•L一1氨水加水稀释,溶液中c(H+)和c(OH-)都减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba2+、Na+、I-、ClO- | B. | K+、Fe2+、SO42-、NO3- | ||
| C. | K+、Mg2+、Br-SO42- | D. | Na+、K+、Clˉ、SiO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 分子式为C7H80且属于酚类物质的同分异构体有4种 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 | |
| D. | 乙酸乙酯中少量乙酸杂质可加饱和Na2C03溶液后经分液除去 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 香兰素的化学式为C8H8O3 | |
| B. | 能与Na2CO3和NaOH溶液反应 | |
| C. | 1 mol香兰素只能与含1 mol Br2的溴水反应 | |
| D. | 能使酸性高锰酸钾溶液褪色的官能团有羟基和醛基 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com