
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ④⑤⑥⑦ | B. | ①②③④⑤⑥ | C. | ①③④⑤ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:解答题
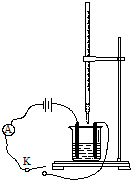 如图,向碱式滴定管和烧杯中分别注入0.2mol•L-1Ba(OH)2溶液和0.1mol•L-1稀硫酸各50mL,并向稀硫酸中滴加几滴石蕊溶液,按如图装置连接好.
如图,向碱式滴定管和烧杯中分别注入0.2mol•L-1Ba(OH)2溶液和0.1mol•L-1稀硫酸各50mL,并向稀硫酸中滴加几滴石蕊溶液,按如图装置连接好.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧化性:Cl2>Fe3+>I2 | B. | 氧化性:Fe3+>I2>Cl2 | ||
| C. | 还原性:I-<Fe2+<Cl- | D. | 还原性:Cl-<I-<Fe2+ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等物质的量的N2和CO所含分子数不一定为NA | |
| B. | S.T.P下22.4L CH4所含电子数目为10NA | |
| C. | 1molF-含质子数与电子数之和为10NA | |
| D. | 1molOH-中所含中子数为8NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ca(ClO)2中Cl元素化合价为-1价 | |
| B. | Ca(OH)2在该反应中失去电子,表现出还原性 | |
| C. | Cl2既是氧化剂又是还原剂 | |
| D. | 若有1molCl2参加反应,则转移2mol电子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,22g CO2含有2NA个氧原子 | |
| B. | 标准状况下,22.4L的CCl4中含有的分子数为NA | |
| C. | 1mol/L的碳酸钠溶液中含Na+离子数为2NA | |
| D. | 常温下,将含0.1NA个HCl分子的氯化氢气体溶于水配成100mL溶液,所得溶液中C(H+)为1mol/L |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 14C与 12C互称同位素;O2与O3是氧元素的同素异形体 | |
| B. | 钢铁生锈主要发生吸氧腐蚀,镀锌铁皮镀层破损后对铁失去保护作用 | |
| C. | 石油的分馏、煤的干馏、电解质溶液导电均属于物理变化 | |
| D. | SO2和NO2属于酸性氧化物,Na2O和Fe3O4属于碱性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com