
科目: 来源: 题型:多选题
 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:X(g)+3Y(g)?2Z(g)△H=-192kJ•mol-1.向M、N中都通入a mol X和b mol Y的混合气体,初始时M、N两容器的容积相同,保持两容器的温度相同且恒定不变.下列说法一定正确的是( )| A. | 平衡时,X的体积分数:M<N | |
| B. | 若向N中再充入a mol X和b mol Y,则平衡时,X的转化率:M<N | |
| C. | 若a:b=1:3,当M中放出172.8 kJ热量时,X的转化率为90% | |
| D. | 若a=1.2,b=1,并且N中达到平衡时体积为2 L,此时含有0.4 mol Z,则再通入0.36 mol X时,v(正)<v(逆) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.2 mol•L-1 | B. | 1.6 mol•L-1 | C. | 2.4 mol•L-1 | D. | 3.6 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HA是弱酸 | B. | HA的电离方程式为HA═H++A- | ||
| C. | 该溶液中c(HA)+c(A-)=0.1 mol•L-l | D. | NaA溶液呈碱性 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2 反应情况 | 点燃时 易化合 | 加热化合 | 加热难 化合 | 不能直 接化合 |
查看答案和解析>>
科目: 来源: 题型:解答题
 A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:查看答案和解析>>
科目: 来源: 题型:解答题
 ;元素C在周期表中的位置是第二周期第VA族,A与B所形成的化合物BA4的电子式为
;元素C在周期表中的位置是第二周期第VA族,A与B所形成的化合物BA4的电子式为 ;
;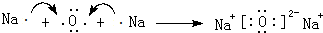 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 100mL0.5mol•L-1MgCl2溶液 | B. | 200mL0.25mol•L-1AlCl3溶液 | ||
| C. | 50mL1mol•L-1NaCl溶液 | D. | 25mL0.5mol•L-1HCl溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
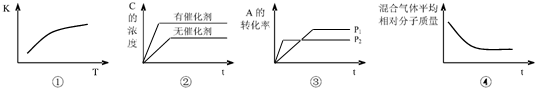
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com