
科目: 来源: 题型:选择题
| A. | SO2通入过量的氨水中:SO2+NH3•H2O═NH4++HSO3- | |
| B. | FeO溶于过量稀硝酸中:FeO+2H+═Fe2++H2O | |
| C. | NH4Al(SO4)2溶液中加入过量NaOH溶液中:NH4++Al3++4OH-═NH3•H2O+Al(OH)3↓ | |
| D. | 铜溶于酸化的H2O2溶液中:Cu+H2O2+2H+═Cu2++2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol Cl2参加反应,转移的电子数目一定为0.2NA | |
| B. | 1.4g聚乙烯中含C-H数目为0.2NA | |
| C. | 标准状况下,5.6L甲醇中含有的分子数目为0.2NA | |
| D. | 常温下,pH=13的NaOH溶液中含OH-的数目为0.1NAA |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 用装置甲制取二氧化硫气体 | |
| B. | 用装置乙收集二氧化硫气体 | |
| C. | 用适量CuO粉末中和反应后溶液,用装置丙过滤 | |
| D. | 用装置丁蒸发浓缩CuSO4溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 测定溶液pH时,pH试纸先用蒸馏水润湿 | |
| B. | 蒸馏实验中,蒸馏前必须在蒸馏烧瓶中加入碎瓷片 | |
| C. | 用盐酸滴定滴定氨水实验中,用甲基橙作指示剂以减小实验误差 | |
| D. |  用如图所示的方法排除碱式滴定管胶管中的气泡 用如图所示的方法排除碱式滴定管胶管中的气泡 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氟化氧分子电子式: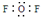 | |
| B. | 质子数与中子数相等的硫原子${\;}_{16}^{16}$S | |
| C. | 镁离子的结构示意图: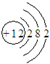 | |
| D. | 对甲基苯酚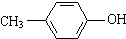 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 澄清石灰水中滴加少量的小苏打溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O | |
| C. | 过氧化钠和水反应:2O22-+2H2O═4OH-+O2↑ | |
| D. | H2O2溶液中滴加酸性KMnO4溶液:2MnO4-+5 H2O2+6H+═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 用饱和食盐水除去Cl2中少量的HCl | |
| B. | 往溴水中通入SO2,可检验SO2的还原性和漂白性 | |
| C. | 往溶液加入盐酸,产生无色无味且能使澄清石灰水浑浊的气体,该气体一定是CO2 | |
| D. | 用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe3+有氧化性,实验室常用KSCN溶液检验Fe3+ | |
| B. | SO2有较强的还原性,SO2可使酸性KMnO4溶液褪色 | |
| C. | Mg有还原性,电解MgCl2饱和溶液可制备Mg | |
| D. | 浓H2SO4有吸水性,浓H2SO4可使蔗糖炭化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com