
科目: 来源: 题型:选择题
| A. | 加入盐酸产生无色气体的溶液中一定含有CO32- | |
| B. | 加入BaCl2溶液产生不溶于稀硝酸的白色沉淀的溶液中一定含有SO42- | |
| C. | 先加足量稀硝酸酸化再加入AgNO3溶液产生白色沉淀的溶液中含有Cl- | |
| D. | 加入无色酚酞溶液仍显无色的溶液一定显酸性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaCl溶液(Na2SO4)加入适量Ba(NO3)2溶液后,过滤 | |
| B. | NaNO3溶液(NaCl)加入适量AgNO3溶液后,过滤 | |
| C. | NaCl溶液(CaCl2)加入适量Na2CO3溶液后,过滤 | |
| D. | NaCl溶液(碘I2)加入四氯化碳后,分液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | n(KOH)=n(KHCO3) | B. | n(KOH)<n(KHCO3) | C. | n(KOH)>n(KHCO3) | D. | KOH、KHCO3任意比 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{1}{3}$mol | B. | $\frac{4}{3}$mol | C. | 1mol | D. | 2mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下22.4LCO2分子数少于NA | B. | 1molNaHCO3固体中含有NA个CO32- | ||
| C. | NA个NO与NA个O2混合分子数为2NA | D. | 1molCu反应转移电子数一定是2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含金属元素的离子不一定是阳离子 | |
| B. | 金属与盐溶液反应都是置换反应 | |
| C. | 玻璃是氧化物,成分可表示成Na2O.CaO.6SiO2 | |
| D. | 与强酸、强碱都反应的物质只有两性氧化物和两性氢氧化物 |
查看答案和解析>>
科目: 来源: 题型:解答题

 .
.
 .
. .
.查看答案和解析>>
科目: 来源: 题型:解答题

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
查看答案和解析>>
科目: 来源: 题型:解答题
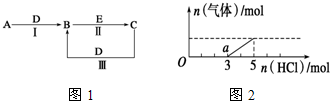
 .②写出反应Ⅰ的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
.②写出反应Ⅰ的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.查看答案和解析>>
科目: 来源: 题型:选择题
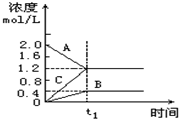 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )| A. | t1时刻之后,若再加入一定量的A,达平衡时A的转化率降低 | |
| B. | t1时刻之后,3v(A)逆=2v(C)正 (v-速率) | |
| C. | t1时刻之后,若升高温度,混合气体的平均摩尔质量增大,则该反应A消耗的方向为吸热反应 | |
| D. | 在温度和容积固定不变的条件下,起始投入1molB、3molC达平衡时A的体积分数为3/7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com