
科目: 来源: 题型:阅读理解
 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:
下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:查看答案和解析>>
科目: 来源: 题型:
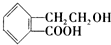 ,它可通过不同的化学反应分别制得B、C和D三种物质:
,它可通过不同的化学反应分别制得B、C和D三种物质: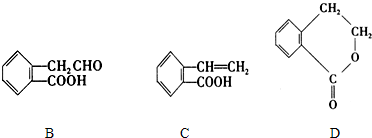
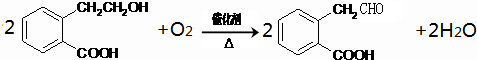



查看答案和解析>>
科目: 来源: 题型:阅读理解

| 16a |
| 22.4b |
| 16a |
| 22.4b |
| 高温高压 |
| 催化剂 |
| 高温高压 |
| 催化剂 |
查看答案和解析>>
科目: 来源: 题型:





查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 如图所示,杠杆A、B两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,小心地向水槽中滴入CuSO4浓溶液.(该过程中不考虑两球浮力的变化)下列说法正确的是( )
如图所示,杠杆A、B两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,小心地向水槽中滴入CuSO4浓溶液.(该过程中不考虑两球浮力的变化)下列说法正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com