
科目: 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
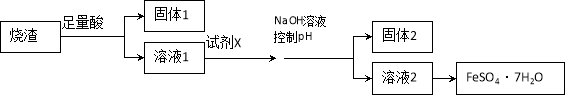
下列说法不正确的是
A.溶解烧渣选用足量硫酸,目的是提高浸出率
B.固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C.从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
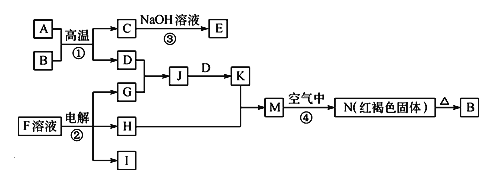
请回答下列问题:
(1)B的化学式为 。
(2)H的电子式为 。
(3)写出反应②的离子方程式 。
(4)写出反应④的化学方程式 。
(5)D是目前应用最广泛的金属,D与炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过该混合物,在微电池 极上Cr2O72–转化为Cr3+,其电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:

(1)写出浸取过程中Cu2S溶解的离子方程式 。
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是 、 。
(3)保温除铁过程中加入CuO的目的是 。
(4)A步操作为 要用硝酸调节溶液的pH,其理由是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验对应的现象及结论均正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 将SO2通入BaCl2溶液, 然后滴入稀硝酸 | 白色沉淀,白色沉淀 不溶于稀硝酸 | 所得沉淀为BaSO3, 后转化为BaSO4 |
B | 浓硫酸滴入蔗糖中, 并搅拌 | 得黑色蓬松的固体并 有刺激性气味气体 | 该过程中浓硫酸仅体 现吸水性和脱水性 |
C | 向FeCl2溶液中加入足 量Na2O2粉末 | 出现红褐色沉淀和 无色气体 | FeCl2溶液部分变质 |
D | 向足量含淀粉的FeI2溶 液中滴加2滴氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
查看答案和解析>>
科目: 来源: 题型:
【题目】有等体积、等pH的Ca(OH)2、KOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A. V3>V2=V1 B. V3=V2=V1 C. V3>V2>V1 D. V1=V2>V3
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法不正确的是( )
A. 福尔马林可浸制标本,因其可使蛋白质变性的性质
B. 向牛奶中加入果汁会产生沉淀,这是因为发生了酸碱中和反应
C. 将地沟油制成肥皂,可以提高资源的利用率
D. 用CO2合成聚碳酸酯可降解塑料,实现碳的循环利用
查看答案和解析>>
科目: 来源: 题型:
【题目】原计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素是19177Ir,则其核内的中子数与质子数之差是( )
A. 77 B. 37 C. 191 D. 114
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化合物依次属于酸、碱、盐、氧化物的是 ( )
A. NaHSO4、KOH、AgCl、CO B. H2CO3、Fe(OH)3、Na2CO3、H2O
C. NH3、H2O2、K2SO4、NO2 D. HCl、Cu2(OH)2CO3、Fe2O3、MnO2
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑和6 mol/L的稀硫酸,其他试剂任选。

请回答下列问题:
(1)B装置中盛有一定量的NaOH溶液,A装置中应预先加入的试剂是________,A装置中发生反应的离子方程式是___________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述制取Fe(OH)2的操作过程__________________。
(4)实验完毕,拔去B装置中的橡胶塞,放入一部分空气,此时B装置中发生反应的化学方程式为_______________________。
(5)在下图中,装置________(填序号)能较长时间观察到Fe(OH)2白色沉淀。

查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三位同学按下列方法制取氢氧化铝,请你参与并回答有关问题。
甲:用可溶性铝盐与稀氨水反应制取氢氧化铝。写出该反应的离子方程式: 。
乙:根据右图电解装置制取氢氧化铝。请回答:

(1) 电源中A极是 极,铝极的电极反应式为 ;
(2)从原理分析,电解质NaCl的作用是 。
丙:利用铝屑、稀H2SO4、NaOH溶液为主要原料制取Al(OH)3固体。
(1)先设计了如下三种方案:
Ⅰ Al3+→Al(OH)3
Ⅱ Al→AlO2-→Al(OH)3
Ⅲ ![]()
从节省原料的角度分析,你认为最合理的方案是 。(填Ⅰ、Ⅱ或Ⅲ)
(2)设计了如下实验步骤:
①配制500 mL 0.5 molL-1NaOH溶液所用到的仪器有:托盘天平(含砝码)、烧杯、玻璃棒、 ;
②在烧杯A中加入50 mL 0.5 molL-1NaOH溶液,再加入足量铝屑给溶液稍加热。其作用是 ,用蒸馏水把铝屑冲洗,干燥后称其质量为m1 g(全部用于制氢氧化铝);
③在盛有适量稀H2SO4的烧杯B中放入 g(含m1的式子表示)铝屑,充分搅拌使铝屑反应完全;
④在盛有适量浓NaOH溶液的烧杯C中入一定质量的铝屑,充分搅拌使铝屑反应完全。该反应的化学方程式为 ;
⑤将烧杯B和烧杯C中的溶液混合,得到氢氧化铝白色沉淀;
⑥将沉淀过滤、洗涤、干燥得Al(OH)3固体m2 g。
试计算此实验中Al(OH)3的产率是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com