
科目: 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)H﹣H、O = O和O﹣H键的键能分别为: a kJ/mol、b kJ/mol和c kJ/mol。CH3OH(g)的燃烧热为△H=—d kJ/mol。则CO2(g)+3H2(g) = CH3OH(g)+ H2O(l) △H= kJmol﹣1。(用含a、b、c、d的代数式表示)
(2)将CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(l)
CH3OCH3(g)+3H2O(l)
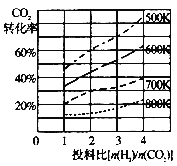
已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示。该反应的△H 0(填“>”或“<”)。若温度不变,减小反应投料比,K值将 (填“增大”、“减小”或“不变”)。
(3)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生反应制备二甲醚,当下列物理量不再发生变化时,能表明上述可逆反应达到化学平衡的是 。(填字母,多选)
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
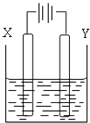
(4)以二甲醚、空气、KOH溶液组成的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,如图所示,请写出该燃料电池负极反应式 。当燃料电池消耗2.8LO2(标况)时,NaCl溶液的pH= (溶液体积变化忽略)(常温)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学小组设计以下实验方案,测定某部分变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
(1)方案一:称取一定质量样品,置于仪器a中用酒精灯加热至恒重,冷却,用托盘天平称量剩余固体质量。重复操作,计算。
仪器a的名称是____________;其中发生反应的化学方程式为_______________。实验中为保证NaHCO3分解完全需加热至恒重,判断方法是________________。
⑵方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,待沉淀后,过滤,洗涤,干燥,称量固体质量,计算。
写出NaHCO3与足量Ba(OH)2溶液反应的离子方程式_______________;实验中判断沉淀是否完全的方法是______________。过滤操作中,除烧杯、漏斗外,还要用到的玻璃仪器为____________。
(3)方案三:称取一定质量样品,按如图装置进行实验:

B装置内所盛试剂是;D装置的作用是______________。实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为________。某同学认为上述测定结果__________(填“偏高”或“偏低”),因为实验装置还存在一个明显的缺陷是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下:

已知:CaO2·8H2O呈白色微溶于水,加热至350℃左右开始分解放出氧气,425℃分解完全。
(1)写出反应①屮氧化还原反应的离子方程式___________________。
(2)向反应①后的溶液中加浓氨水的目的是_________________。
(3)写出反应②的化学方程式_________________;反应②常用冰水控制温度在0℃左右.其可能原因是(写出两种):
①________________;②________________。
(4)测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加人适量蒸馏水和过量的b gKI晶体,再滴人少量2 mol L-1H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加人几滴淀粉溶液。
第三步:逐滴加入浓度为c mol L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。已知:I2+2S2O32- =2I-+S4O62-。
某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能__________(填“不受影响”“偏低”或“偏高”),原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A.每生成2分子AB吸收b kJ热量
B.该反应热ΔH=-(a-b) kJ·mol-1
C.该反应中生成物的总能量高于反应物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表述正确的是
A.0.1 mol/L的(NH4)2SO4溶液:c(SO![]() )>c(NH
)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.0.1 mol/L的NaHCO3溶液:c(Na+)=c(HCO![]() )+c(H2CO3)+2c(CO
)+c(H2CO3)+2c(CO![]() )
)
C.将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得溶液:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.0.02mol/L CH3COOH溶液和0.01 mol/L NaOH溶液等体积混合所得溶液:
2c(H+)+ c(CH3COOH) = c(CH3COO- ) +2c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子的浓度为
A.0.1(b-2a)mol·L-1
B.10(2a-b)mol·L-1
C.10(b-2a)mol·L-1
D.10(b-a)mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色。

如果溶液紫色褪去,说明该样品中含有亚硫酸钠。
(1)用离子方程式表示该反应原理: 。
(2)图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是____________mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填字母)________________。
A.等于amL B.等于(25-a)mL C.大于amL D.大于(25-a)mL
(3)该小组同学欲测定样品中亚硫酸钠的含量,操作步骤如下:
a.称取mg样品,用蒸馏水溶解并置于锥形瓶中
b.将V1mL C1mol/L的酸性KMnO4溶液(过量)倒入锥形瓶中振荡
c.用C2mol/L草酸钠(Na2C2O4)溶液滴定过量的KMnO4,至滴定终点时用去Na2C2O4溶液V2mL
①KMnO4溶液应装在_________式滴定管中,达到滴定终点时溶液颜色的变化 。
②样品中Na2SO3的物质的量为 mol。(用含C1 、V1 、C2、 V2的代数式表示)。
(4)下列操作会导致测得的Na2SO3的物质的量偏高的是 (填字母,双选)。
A.未用Na2C2O4标准液润洗滴定管
B.滴定前仰视盛有Na2C2O4溶液的滴定管,滴定后俯视
C.滴定前滴定管尖嘴处有气泡,滴定后消失
D.滴定时摇动锥形瓶,瓶中的液滴溅出
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是 ( )
A.三氯蔗糖(C12H19Cl3O8)属于天然的糖类甜味剂
B.未成熟的青苹果肉遇碘酒变蓝色,成熟苹果的汁能发生银镜反应
C.利用盐析的方法可以用来分离、提纯蛋白质
D.酚醛树脂、合成橡胶、有机玻璃都属于有机高分子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】关于“碳是生命的核心元素”,“没有碳,就没有生命”的叙述,错误的是( )
A. 碳元素在生物体内含量最多
B. 组成细胞的重要有机物都含有碳元素
C. 组成蛋白质的氨基酸是以若干个相连的碳原子构成的碳链为基本骨架
D. 组成多糖的单糖是以若干个相连的碳原子构成的碳链为基本骨架
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com