
科目: 来源: 题型:
【题目】在容积不变的密闭容器中,在一定条件下发生反应2A(?)![]() B(g)+C(s),达到化学平衡后,其他条件不变,升高温度时,容器内气体的密度增大,则下列叙述正确的是
B(g)+C(s),达到化学平衡后,其他条件不变,升高温度时,容器内气体的密度增大,则下列叙述正确的是
A.若正反应是吸热反应,则A为气态
B.若正反应是放热反应,则A为气态
C.改变压强对平衡的移动无影响
D.在平衡体系中加入少量C,则平衡向逆反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。
(1)在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I- 被氧化为I2时,产物中含氮的物质为____________(填化学式)。
(2)要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是___________(填序号)。
a. 稀硫酸 b. 二氧化碳 c.二氧化硫 d.磷酸
(3)工业废水中的NO2- 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中:
![]()
(4)改用电解法将废水中NO2- 转换为N2除去,N2将在___________(填电极名称)生成
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在pH = 1的溶液中:SO![]() 、Cl、NO
、Cl、NO![]() 、Na+
、Na+
B.在能使酚酞变红的溶液中:Na+、Cl、NO![]() 、K+
、K+
C.在1 mol·L-1的NaAlO2溶液中:K+、Ba2+、SO![]() 、OH
、OH
D.在1 mol·L-1的AlCl3溶液中:NH![]() 、Ag+、Na+、NO
、Ag+、Na+、NO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表示对应的化学反应的离子方程式正确的是( )
A、MnO2与浓盐酸反应制氯气:MnO2+4HCl=Mn2++2Cl-+Cl2↑+2H2O
B、明矾溶于水产生氢氧化铝胶体:Al3++3H2O=Al(OH)3↓+3H+
C、过氧化钠溶于水产生氧气:Na2O2+H2O=2Na++2OH-+O2↑
D、Ca(HCO3)2溶液与少量NaOH溶液反应:OH-+HCO3-+Ca2+=CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。

(1)用离子方程式解释现象I中出现胶状沉淀的原因: 。
(2)II中加碱时出现的现象是 ,此现象说明溶液中发生反应的离子方程式是 。
(3)III中加碱时出现的现象是 。
(4)用离子方程式解释IV中加碱时出现的现象: 。
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。
实验 | 试剂及操作 | 现象 | |
试管 | 滴管 | ||
1.0 mL | 0.1 mol·L1 Fe(NO3)2溶液 | 先滴加1.5 mL 1.0 mol·L1 H2SO4溶液; 再滴加1.0 mL 0.5 mol·L1 NaOH溶液 | V.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 |
①探究加酸时Fe(NO3)2溶液中是否发生了反应:向1.0 mL 0.1 mol·L1 Fe(NO3)2溶液中 ,溶液立即变红,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。
② 推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1 mol·L1 Fe(NO3)2溶液中的Fe2+被NO3-氧化;
b. (用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】煤制天然气工艺是煤高效洁净利用的新途径之一,其工艺流程简图如下:


(1)反应I:C(s)+H2O(g)![]() CO(g)+H2(g)ΔH=+135kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用: 。
CO(g)+H2(g)ΔH=+135kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用: 。
(2)反应II:CO(g)+H2O(g)![]() CO2(g)+H2(g)ΔH=41kJ·mol-1。下图表示不同温度条件下,煤气化反应I发生后的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡转化率的变化关系。
CO2(g)+H2(g)ΔH=41kJ·mol-1。下图表示不同温度条件下,煤气化反应I发生后的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡转化率的变化关系。
①判断T1、T2和T3的大小关系: 。
②若煤气化反应I发生后的汽气比为0.8,经煤气化反应I和水气变换反应II后,得到CO与H2的物质的量之比为1:3,则反应II应选择的温度是 (填“T1”“T2”或“T3”)。
(3)①甲烷化反应IV发生之前需要进行脱酸反应III。煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和 。
②工业上常用热碳酸钾法脱除H2S气体得到两种酸式盐,该反应的化学方程式是 。
(4)已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) H1=41kJ·mol1
CO2(g)+H2(g) H1=41kJ·mol1
2H2(g)+O2(g)![]() 2H2O(g) H2=484kJ·mol1
2H2O(g) H2=484kJ·mol1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) H3=802kJ·mol1
CO2(g)+2H2O(g) H3=802kJ·mol1
反应IV:CO(g)+3H2(g)![]() CH4(g)+H2O(g) H= 。
CH4(g)+H2O(g) H= 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色。则以下说法正确的是

A.电源B极是正极
B.甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶1
C.欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
查看答案和解析>>
科目: 来源: 题型:
【题目】常温常压下断裂1 mol(理想)气体分子化学键所吸收的能量或形成1 mol(理想)气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-F | 427 | C-Cl | 330 | C-I | 218 |
H-H | 436 | S=S | 255 | H-S | 339 |
请完成下列问题。
(1)由表中数据规律预测C-Br键的键能范围:_ <C-Br键能< (填写数值和单位)
(2)热化学方程式2H2(g)+S2(g)=2H2S(g) ΔH= Q kJ·mol-1;则Q= __
(3) 已知下列热化学方程式:
O2 (g) = O![]() (g)+e- ΔH1= +1175.7 kJ·mol-1
(g)+e- ΔH1= +1175.7 kJ·mol-1
PtF6(g)+e-= PtF![]() (g) ΔH2= —771.1 kJ·mol-1
(g) ΔH2= —771.1 kJ·mol-1
O![]() PtF
PtF![]() (s) = O
(s) = O![]() (g)+PtF
(g)+PtF![]() (g) ΔH3= +482.2 kJ·mol-1
(g) ΔH3= +482.2 kJ·mol-1
则反应O2(g) +___ ___(g)=O![]() PtF
PtF![]() (s) ΔH=___ ___kJ·mol-1。
(s) ΔH=___ ___kJ·mol-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
A.增大压强 B.升高温度 C.使用催化剂 D.多充入O2
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
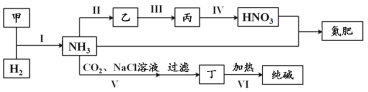
下列说法不正确的是
A.甲、乙、丙三种物质中都含有氮元素
B.反应II、III和Ⅳ的氧化剂相同
C.VI的产物可在上述流程中被再次利用
D.V中发生反应:NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com