
科目: 来源: 题型:
【题目】Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性。可用作医药、抗氧化剂以及制备次磷酸钠等。由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:

步骤1.在三口烧瓶中加入白磷和石灰乳,先通入N2,然后在约98°C下充分搅拌1h,同时收集产生的PH3。
步骤2.将反应液静置、过滤。
步骤3.向滤液中通入适量CO2,再过滤。
步骤4.用次磷酸溶液调节步骤3滤液的pH,浓缩、冷却结晶、干燥得次磷酸钙。
(1)步骤1先通入N2的目的是 ;搅拌的目的是 。
(2)步骤1石灰乳与 P4(白磷)发生反应的化学方程式为 ;步骤2过滤所得滤渣成分为 。
(3)步骤3的目的是 。
(4)请补充完整由产品进一步制备NaH2PO2·H2O的实验方案:取产品次磷酸钙加入烧杯中,加适量的水溶解, ,干燥得到NaH2PO2·H2O。(已知:在常压下,加热蒸发次磷酸钠溶液会发生爆炸,100℃时NaH2PO2·H2O的溶解度为667g/100g水)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:实验室可供选择的用于去除气体杂质的试剂有:浓硫酸、无水氯化钙、五氧化二磷、碱石灰(主要成分为NaOH和CaO)。

实验室用上图所示装置进行纯净干燥的氢气还原氧化铁实验。a装置名称为 ,方框B内应选用下图装置 (填“Ⅰ”或“Ⅱ”),选用的除杂试剂为 (填试剂名称)。

②实验室常用36.5%浓盐酸(ρ=1.2g·cm-3)配制稀盐酸,若要配制500mL,0.5 mol·L-1稀盐酸,需用量筒取用浓盐酸 mL。
③写出装置C中发生反应的化学方程式并用单线桥标明电子的转移 。实验结束时应该采取的操作是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸盐与钴(Ⅲ)形成的一种配合物1Co(NH3)5NO2]Cl2的制备流程如下:
![]()
(1)Co2+基态核外电子排布式为 。
(2)配合物1Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为 (填元素符号);配离子 1Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为 。
(3)与NO2-互为等电子体的单质分子为 (写化学式)。
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为 。
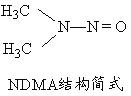
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构简式如图所示,1molNDMA分子中含有![]() 键的数目为 mol。
键的数目为 mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】据《参考消息》报道,有科学家提出硅是“21世纪的能源”“未来的石油”的观点。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s) ΔH=-989.2 kJ·mol-1,有关键能数据如下表:
化学键 | Si—O | O=O | Si—Si |
键能(kJ/mol) | x | 498.8 | 176 |
已知1 mol Si中含2 mol Si—Si键,1 mol SiO2中含4 mol Si—O键,则x的值为____________。
(2)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是________________。
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(3)工业制备纯硅的反应为2H2(g)+SiCl4(g)=Si(s)+4HCl(g) ΔH=+240.4 kJ·mol-1,
生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应,则反应过程中__________(填“吸收”或“释放”)的热量为________kJ。
查看答案和解析>>
科目: 来源: 题型:
【题目】在101 kPa时,1 g CH4完全燃烧生成CO2和液态H2O,放出55.64 kJ的热量。
(1)写出CH4燃烧热表示的热化学方程式。
(2)1000 L CH4(标准状况)燃烧后所产生的热量为多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】硫、氮、碳的氧化物都会引起环境问题,越来越引起人们的重视,如图1是氮元素的各种价态与物质类别的对应关系

(1)根据A对应的化合价和物质类别,A为 (写分子式),从氦元素的化合价能否发生变化的角度判断,图1中既有氧化性又有还原性的化合物是 ;
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为 ;
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式 ;
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为 ;
A 双氧水(H2O2) B品红溶液 C 酸性高猛酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】碘化钡(BaI2·2H2O)是一种白色粉末,常用于制取其他含碘化合物。一种制备流程如下:

(1)步骤Ⅰ制FeI2溶液时,提高反应速率的可行措施有 (填序号)。
a.铁粉和碘粉用球磨机磨成细粉
b.增大n(铁粉)∶n(碘)的配料比
c.适当升高反应温度和搅拌速度
d.向反应器中加水至I2全部溶解
(2)步骤Ⅱ发生反应的化学方程式为 ;用pH试纸测定溶液pH的方法是 。
(3)步骤Ⅲ小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是 ;步骤V加入活性炭的目的是 。
(4)从过滤2所得滤液中获得BaI2·2H2O(溶解度曲线如右图所示)的方法是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在“分子马达”研究方面的成就,一种光驱分子马达结构如下图所示。有关该分子的说法正确的是

A. 该分子中有两个手性碳原子 B. 两个苯环可以处于同一平面
C. 能与NaHCO3和酸性KMnO4溶液反应 D. 1mol该分子最多可与2molH2发生加成
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素M和N的离子M2+和N2-具有相同电子层结构,则下列说法正确的是
A. M原子比N原子多一个电子层
B. M的原子序数比N小
C. M和N原子的电子层数相等
D. M和N原子最外层电子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com