
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–¬»‘ΣΥΊΚ§―θΥαΥα–‘Ήν»θΒΡ «
A. HClO4 B. HClO3 C. HClO2 D. HClO
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ ÷–Θ§Φ»Κ§”–άκΉ”ΦϋΘ§”÷Κ§”–Ζ«ΦΪ–‘Ι≤ΦέΦϋΒΡ «
A. Na2O2 B. CaCl2 C. NH4Cl D. H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ«χ±πΨßΧε”κΖ«ΨßΧεΒΡΉνΩΤ―ßΒΡΖΫΖ® «
A. Ιέ≤λΗςœρ“λ–‘ B. X…δœΏœΈ…δ Β―ι C. ≤βΕ®ΙΧΕ®»έΒψ D. Ιέ≤λΉ‘ΖΕ–‘
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉΆ§―ßΫχ––Fe2+ΜΙ‘≠–‘ΒΡ Β―ιΘ§’κΕ‘“λ≥Θœ÷œσΫχ––ΧΫΨΩΓΘ
≤Ϋ÷η“ΜΘΚ÷Τ»ΓFeCl2»ή“ΚΘ°œρ0.1molΓΛL-1 FeCl3»ή“Κ÷–Φ”ΉψΝΩΧζΖέ’ώΒ¥Θ§Ψ≤÷ΟΚσ»Γ…œ≤ψ«ε“ΚΘ§≤βΒΟpHΘΦ1ΓΘ
Β―ιΕΰΘΚœρ2mL FeCl2»ή“Κ÷–ΒΈΦ”2ΒΈ0.1molΓΛL-1KSCN»ή“ΚΘ§Έόœ÷œσΘΜ‘ΌΒΈΦ”5ΒΈ5% H2O2»ή“Κ(Έο÷ ΒΡΝΩ≈®Ε»‘ΦΈΣ1.5molΓΛL-1ΓΔpH‘ΦΈΣ5)Θ§Ιέ≤λΒΫ»ή“Κ±δΚλΘ§¥σ‘Φ10ΟκΉσ”“Κλ…ΪΆ »ΞΘ§”–ΤχΧε…ζ≥…(Ψ≠Φλ―ιΈΣO2)Θ°
Θ®1Θ©”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ≤Ϋ÷ηΕΰ÷–»ή“Κ±δΚλΒΡ‘≠“ρΘΚ________________ΓΘ
Θ®2Θ©ΦΉΧΫΨΩ≤Ϋ÷ηΕΰ÷–»ή“ΚΆ …ΪΒΡ‘≠“ρΘΚ
Δώ.»ΓΆ …ΪΚσ»ή“ΚΝΫΖίΘ§“ΜΖίΒΈΦ”FeCl3»ή“ΚΈόœ÷œσΘΜΝμ“ΜΖίΒΈΦ”KSCN»ή“Κ≥ωœ÷Κλ…ΪΘΜ
Δρ.»ΓΆ …ΪΚσ»ή“ΚΘ§ΒΈΦ”―ΈΥαΚΆBaCl2»ή“ΚΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΓΘ
Δσ.œρ2mL 0.1molΓΛL-1 FeCl3»ή“Κ÷–ΒΈΦ”2ΒΈ0.1molΓΛL-1KSCN»ή“ΚΘ§±δΚλΘ§Ά®»κO2Θ§ΈόΟςœ‘±δΜ·ΓΘ
ΔΌ Β―ιIΒΡΥΒΟς__________________ΘΜ
ΔΎ Β―ιΔσΒΡΡΩΒΡ «____________________ΓΘ
ΒΟ≥ωΫα¬έΘΚ»ή“ΚΆ …ΪΒΡ‘≠“ρ «Υα–‘ΧθΦΰœ¬H2O2ΫΪSCN-―θΜ·≥…SO42-ΓΘ
Θ®3Θ©ΔΌΦΉ÷±Ϋ””ΟFeCl2ΓΛ4H2O≈δ÷Τ_________molΓΛL-1ΒΡFeCl2»ή“ΚΘ§÷ΊΗ¥≤Ϋ÷ηΕΰ÷–ΒΡ≤ΌΉςΘ§ΖΔœ÷“ΚΧεΚλ…Ϊ≤ΔΈ¥Ά »ΞΘ§Ϋχ“Μ≤ΫΧΫΨΩΤδ‘≠“ρΘΚ
ΔΎ.”ΟΦΛΙβ± Ζ÷±π’’…δΚλ…Ϊ“ΚΧεΚΆΒΈΦ”ΝΥKSCN»ή“ΚΒΡFeCl3»ή“ΚΘ§«Α’Ώ”–ΕΓ¥οΕϊ–ß”ΠΘ§Κσ’ΏΈόΘ°≤βΥυ≈δFeCl2»ή“ΚΒΡpH‘ΦΈΣ3Θ°”…¥ΥΘ§““»œΈΣΚλ…Ϊ≤ΜΆ »ΞΒΡΩ…Ρή‘≠“ρ «ΘΚ____________________ΓΘ
Δέ.≤ι‘ΡΉ ΝœΚσΆΤ≤βΘ§Κλ…Ϊ≤ΜΆ »ΞΒΡ‘≠“ρΜΙΩ…Ρή «pHΫœ¥σ ±H2O2≤ΜΡή―θΜ·SCN-Θ°““άϊ”Ο…œ ω≤ΩΖ÷ ‘ΦΝΘ§Ά®Ιΐ Β―ι≈≈≥ΐΝΥ’β“ΜΩ…ΡήΘ°““ΒΡ Β―ι≤ΌΉςΦΑœ÷œσ «ΘΚ
≤Ϋ÷η | ‘ΦΝΦΑ≤ΌΉς | œ÷ œσ |
i | …ζ≥…ΑΉ…Ϊ≥ΝΒμ | |
ii | œρiΥυΒΟ»ή“Κ÷–ΒΈΦ”0.1molΓΛL-1 FeCl3»ή“Κ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΩ…ΡφΖ¥”ΠΘΚ2NO2![]() 2NOΘΪO2‘ΎΚψ»ίΒΡΟή±’»ίΤς÷–Ϋχ––Θ§¥οΒΫΤΫΚβΉ¥Χ§ΒΡ±ξ÷Ψ «Θ® Θ©
2NOΘΪO2‘ΎΚψ»ίΒΡΟή±’»ίΤς÷–Ϋχ––Θ§¥οΒΫΤΫΚβΉ¥Χ§ΒΡ±ξ÷Ψ «Θ® Θ©
ΔΌΒΞΈΜ ±ΦδΡΎ…ζ≥…n mol O2ΒΡΆ§ ±…ζ≥…2n mol NO2
ΔΎΒΞΈΜ ±ΦδΡΎ…ζ≥…n mol O2ΒΡΆ§ ±…ζ≥…2n mol NO
Δέ”ΟNO2ΓΔNOΓΔO2±μ ΨΒΡΖ¥”ΠΥΌ¬ ΒΡ±»ΈΣ2ΓΟ2ΓΟ1ΒΡΉ¥Χ§
ΔήΜλΚœΤχΧεΒΡ―’…Ϊ≤Μ‘ΌΗΡ±δΒΡΉ¥Χ§
ΔίΜλΚœΤχΧεΒΡΟήΕ»≤Μ‘ΌΗΡ±δΒΡΉ¥Χ§
ΔόΜλΚœΤχΧεΒΡ―Ι«Ω≤Μ‘ΌΗΡ±δΒΡΉ¥Χ§
ΔΏΜλΚœΤχΧεΒΡΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ≤Μ‘ΌΗΡ±δΒΡΉ¥Χ§
AΘ°ΔΌΔήΔόΔΏ BΘ°ΔΎΔέΔίΔΏ CΘ°ΔΌΔέΔήΔί DΘ°»Ϊ≤Ω
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΑ±ΒΡΜ·ΚœΈοΚœ≥…ΓΔ”Π”ΟΦΑΑ±ΒΡΙΧΕ®“Μ÷± «ΩΤ―ß―–ΨΩΒΡ»»ΒψΓΘ
Θ®1Θ©“‘CO2”κNH3ΈΣ‘≠ΝœΚœ≥…Μ·Ζ ΡρΥΊΒΡ÷ς“ΣΖ¥”Π»γœ¬ΘΚ
ΔΌ2NH3(g)ΘΪCO2(g)ΘΫNH2CO2NH4(s)ΘΜΠΛHΘΫΘ≠159.47kJΓΛmol-1
ΔΎNH2CO2NH4(s)ΘΫCO(NH2)2(s)ΘΪH2O(g)ΘΜΠΛHΘΫakJΓΛmol-1
Δέ2NH3(g)ΘΪCO2(g)ΘΫCO(NH2)2(s)ΘΪH2O(g)ΘΜΠΛHΘΫΘ≠86.98kJΓΛmol-1
‘ρaΈΣ______________ΓΘ
Θ®2Θ©Ζ¥”Π2NH3(g)ΘΪCO2(g)![]() CO(NH2)2(l)ΘΪH2O(g)‘ΎΚœ≥…Υΰ÷–Ϋχ––ΓΘœ¬ΆΦ÷–ΔώΓΔΔρΓΔΔσ»ΐΧθ«ζœΏΈΣΚœ≥…Υΰ÷–Α¥≤ΜΆ§Α±ΧΦ±» [n(NH3)/n(CO2)]ΚΆΥ°ΧΦ±»[n(H2O)/n(CO2)]ΆΕΝœ ±Εΰ―θΜ·ΧΦΉΣΜ·¬ ΒΡ«ιΩωΓΘ
CO(NH2)2(l)ΘΪH2O(g)‘ΎΚœ≥…Υΰ÷–Ϋχ––ΓΘœ¬ΆΦ÷–ΔώΓΔΔρΓΔΔσ»ΐΧθ«ζœΏΈΣΚœ≥…Υΰ÷–Α¥≤ΜΆ§Α±ΧΦ±» [n(NH3)/n(CO2)]ΚΆΥ°ΧΦ±»[n(H2O)/n(CO2)]ΆΕΝœ ±Εΰ―θΜ·ΧΦΉΣΜ·¬ ΒΡ«ιΩωΓΘ

ΔΌ«ζœΏΔώΓΔΔρΓΔΔσΥ°ΧΦ±»ΒΡ ΐ÷ΒΖ÷±πΈΣΘΚ
AΘ°0.6ΓΪ0.7 BΘ°1ΓΪ1.1 CΘ°1.5ΓΪ1.61
…ζ≤ζ÷–”Π―Γ”ΟΥ°ΧΦ±»ΒΡ ΐ÷ΒΈΣ ___________(―ΓΧν–ρΚ≈)ΓΘ
ΔΎ…ζ≤ζ÷–Α±ΧΦ±»“ΥΩΊ÷Τ‘Ύ4.0Ήσ”“Θ§Εχ≤Μ «4.5ΒΡ‘≠“ρΩ…Ρή « ΓΘ
Θ®3Θ©ΡρΥΊΩ…”Ο”Ύ ΣΖ®―ΧΤχΆ―ΒΣΙΛ“’Θ§ΤδΖ¥”Π‘≠άμΈΣΘΚ
NOΘΪNO2ΘΪH2OΘΫ2HNO2ΘΜ2HNO2ΘΪCO(NH2)2ΘΫ2N2ΓϋΘΪCO2ΓϋΘΪ3H2OΓΘ
ΔΌΒ±―ΧΤχ÷–NOΓΔNO2Α¥…œ ωΖ¥”Π÷–œΒ ΐ±» ±Ά―ΒΣ–ßΙϊΉνΦ―ΓΘ»τ―ΧΤχ÷–V(NO)ΓΟV(NO2)ΘΫ5ΓΟ1 ±Θ§Ω…Ά®»κ“ΜΕ®ΝΩΒΡΩ’ΤχΘ§Ά§Έ¬Ά§―Ιœ¬Θ§V(Ω’Τχ)ΓΟV(NO)ΘΫ (Ω’Τχ÷–―θΤχΒΡΧεΜΐΚ§ΝΩ¥σ‘ΦΈΣ20%)ΓΘ
ΔΎœ¬ΆΦ «ΡρΥΊΚ§ΝΩΕ‘Ά―ΒΣ–ß¬ ΒΡ”ΑœλΘ§¥”Ψ≠ΦΟ“ρΥΊ…œΩΦ¬«Θ§“ΜΑψ―Γ‘ώΡρΥΊ≈®Ε»‘ΦΈΣ_________%ΓΘ

Θ®4Θ©œ¬ΆΦ±μ Ψ Ι”Ο–¬–ΆΒγΦΪ≤ΡΝœΘ§“‘N2ΓΔH2ΈΣΒγΦΪΖ¥”ΠΈοΘ§“‘HClΘ≠NH4ClΈΣΒγΫβ÷ »ή“Κ÷Τ‘λ≥ωΦ»ΡήΧαΙ©ΡήΝΩΘ§Ά§ ±”÷Ρή Βœ÷ΒΣΙΧΕ®ΒΡ–¬–Ά»ΦΝœΒγ≥ΊΓΘ«κ–¥≥ωΗΟΒγ≥ΊΒΡ’ΐΦΪΖ¥”Π Ϋ___________________ΓΘ…ζ≤ζ÷–Ω…Ζ÷άκ≥ωΒΡΈο÷ AΒΡΜ·―ß ΫΈΣ ΓΘ

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘”ΎΖ¥”ΠΘΚ2XΘ®gΘ©ΘΪYΘ®gΘ© ![]() 2ZΘ®gΘ©‘Ύ≤ΜΆ§Έ¬Ε»Θ®T1ΚΆT2Θ©ΦΑ―Ι«ΩΘ®p1ΚΆp2Θ©œ¬Θ§≤ζΈοZΒΡΈο÷ ΒΡΝΩnΘ®ZΘ©ΚΆΖ¥”Π ±ΦδtΒΡΙΊœΒ»γ”“ΆΦΥυ ΨΘ§œ¬Ν–≈–Εœ’ΐ»ΖΒΡ «Θ® Θ©
2ZΘ®gΘ©‘Ύ≤ΜΆ§Έ¬Ε»Θ®T1ΚΆT2Θ©ΦΑ―Ι«ΩΘ®p1ΚΆp2Θ©œ¬Θ§≤ζΈοZΒΡΈο÷ ΒΡΝΩnΘ®ZΘ©ΚΆΖ¥”Π ±ΦδtΒΡΙΊœΒ»γ”“ΆΦΥυ ΨΘ§œ¬Ν–≈–Εœ’ΐ»ΖΒΡ «Θ® Θ©
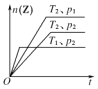
AΘ°T1ΘΦT2Θ§p1ΘΦp2Θ§’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π
BΘ°T1ΘΨT2Θ§p1ΘΨp2Θ§’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”Π
CΘ°T1>T2Θ§p1ΘΨp2Θ§’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π
DΘ°T1ΘΨT2Θ§p1ΘΦp2Θ§’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”Π
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ¥”Ϋπ τάϊ”ΟΒΡάζ ΖΩ¥Θ§œ» ««ύΆ≠Τς ±¥ζΘ§ΕχΚσ «ΧζΤς ±¥ζΘ§¬ΝΒΡ“±ΝΕ «ΫϋΑΌΡξΒΡ ¬Θ°ΨωΕ®Ϋπ τ Ι”ΟΡξ¥ζœ»ΚσΥ≥–ρΒΡΙΊΦϋ“ρΥΊ «Θ® Θ©
A.Ϋπ τΒΡΜνΕ·–‘
B.Ϋπ τΒΡΒΦΒγ–‘
C.Ϋπ τΒΡ―”’Ι–‘
D.ΒΊΩ«÷–Ϋπ τ‘ΣΥΊΒΡΚ§ΝΩ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2014Ρξ «Ο≈ΫίΝ–ΖρΒ°≥Ϋ180÷ήΡξΘ§œ¬Ν– ¬ Β≤ΜΡή”Ο‘ΣΥΊ÷ήΤΎ¬…Ϋβ ΆΒΡ”–Θ® Θ©
A.Φν–‘ΘΚKOHΘΨNaOH
B.»ήΫβΕ»ΘΚSO2ΘΨCO2
C.Υα–‘ΘΚHClO4ΘΨH2SO4
D.ΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘ΘΚH2OΘΨNH3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΉ–œΗΖ÷Έωœ¬Ν–±μΗώ÷–ΧΰΒΡ≈≈Ν–Ιφ¬…Θ§≈–Εœ≈≈Ν–‘ΎΒΎ16ΈΜΧΰΒΡΖ÷Ή” Ϋ «Θ® Θ©
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | Γ≠ |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | Γ≠ |
A.C6H12
B.C6H14
C.C7H12
D.C7H14
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com