
科目: 来源: 题型:
【题目】矿盐(主要成分是NaCl,还含有SO![]() 等其他可溶性杂质的离子),下列有关说法正确的是
等其他可溶性杂质的离子),下列有关说法正确的是
A.由矿盐生产食盐,除去SO![]() 最合适的试剂是Ba(NO3)2
最合适的试剂是Ba(NO3)2
B.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
C.侯氏制碱法中,向饱和在食盐水中先通入二氧化碳,然后再通入氨气
D.工业上通过电解氯化钠溶液制备金属钠和氯气
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
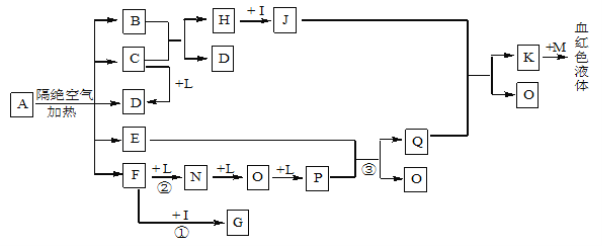
(1)写出D的电子式为_______________;
(2)写出反应①的化学方程式: ;写出反应②的化学方程式: ;反应③中氧化剂和还原剂的物质的量之比为_________________;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为 ______________________;
(4)检验J中阳离子的实验方法为 ;
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C): n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为_________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
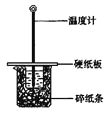
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”,下同) 若用KOH代替NaOH,测定结果会 __ __
(5)他们记录的实验数据如下:
实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
t1 | t2 | ||||
① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
已知反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。
①计算完成上表。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是 ( )
A.标准状况下,1mol石墨的体积约是22.4L
B.常温常压下,44 g CO2和28 g CO所占的体积相同
C.非标准状况下,1mol任何气体的体积都不可能是22.4L
D.当微粒数目相同时,气体物质的体积主要决定于微粒本身的大小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列家庭小实验中不涉及化学变化的是
A. 用铁钉等材料探究铁生锈的条件 B. 用糯米、酒曲和水制甜酒
C. 用75%的酒精杀菌消毒 D. 用木炭除去冰箱中的异味
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ___________(2)除去食盐溶液中的水 ___________
(3)淡化海水 ___ ______ (4)KCl中含有KClO3 。
Ⅱ.根据以下装置图,回答下列问题:

写出仪器名称 ② ③ ;仪器①~④中,使用时必须检查是否漏水的有 (填序号)。
Ⅲ.某课外活动小组设计下列实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
(1)过氧化钠与水反应的化学方程式是 。
(2)装置Ⅰ是制备纯净的 ,则仪器①和②中最适宜的试剂组合是________(填字母)
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2,关闭K1,观察到预期现象后,打开K1 ,再关闭K2。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是 ;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是 。
(5)为进一步达到实验目的,应补充的实验是:取最终反应后Ⅲ中所得固体, 。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.合成氨的原料气H2可通过反应CO(g)+H2O(g)![]() CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
(1)T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 。
(2)保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入固定容器中进行反应,下列描述
能够说明体系处于平衡状态的是 (填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成amolCO2的同时消耗amolH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
II.液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧实验中相关的反应有:
① 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H1
② 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H2
③ 4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H3
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
III.(1)右图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。由图可知Mg与卤素单质的反应均为 (填“放热”或“吸热”)反应。
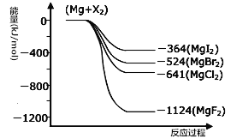
(2)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体(CH4)和沉淀生成。写出CH3MgCl水解的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应。现将2 mol SO2 、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%。下列热化学方程式正确的是
A.2SO3(g)![]() 2SO2(g)+O2(g);△H =+196.6 kJ/mol
2SO2(g)+O2(g);△H =+196.6 kJ/mol
B.2SO2(g)+O2(g)![]() SO3(g);△H =-98.3 kJ/mol
SO3(g);△H =-98.3 kJ/mol
C.SO2(g)+1/2O2(g)![]() SO3(g);△H=+98.3 kJ/mol
SO3(g);△H=+98.3 kJ/mol
D.SO2(g)+1/2O2(g)![]() SO3(g);△H=-196.6 kJ/mol
SO3(g);△H=-196.6 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com