
科目: 来源: 题型:
【题目】下列说法正确的是
A. 原子晶体中只存在共价键
B. 非金属元素形成的化合物不能形成离子晶体
C. 干冰升华时,分子内共价键会发生断裂
D. 金属元素和非金属元素形成的化合物一定是离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS。某同学用15.0 g该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:
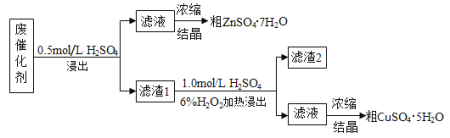
已知:ZnS与稀硫酸反应,且化合价不变;CuS不与稀硫酸反应。回答下列问题:
(1)在下列装置中,第一次浸出必须用 。(填标号)
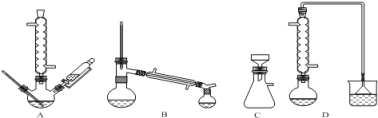
(2)第二次浸出时,向盛有滤渣1的反应器中先加入稀H2SO4,后滴入H2O2溶液。
①写出第二次浸出(有单质生成)的化学方程式 。
②若滴加H2SO4和H2O2顺序相反,会造成 。
③滤渣2的主要成分是 。
CuS+H2O2+H2SO4=CuSO4+S+2H2O
(3)浓缩硫酸锌、硫酸铜溶液使用的主要仪器名称是 。
(4)该同学在实验完成之后,得到1.50g CuSO4·5H2O,则铜的回收率为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用下图所示装置制备AlCl3溶液,并用AlCl3溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后煅烧沉淀制备新型的超导材料和发光材料七铝十二钙(12CaO·7Al2O3)。已知AlCl3易水解,易升华。

(1)实验室用氯酸钾和浓盐酸制备氯气,其离子方程式为 ;C装置的作用 。
(2)氯气与废铝屑反应生成的AlCl3蒸气溶解在B中浓盐酸,为了防止AlCl3蒸气凝华堵塞导管,实验中可采取的措施是 (写出一点)。
(3)AlCl3溶液溶解CaCO3时,AlCl3溶液和碳酸钙粉末的混合方式为 。
(4)实验要控制碳酸钙和AlCl3的量,要求n(CaCO3)∶n(AlCl3)> 。
(5)用白云石(主要成分为CaCO3、MgCO3)制备纯净碳酸钙的实验方案为:将一定量的白云石煅烧, 。(实验中需用到的试剂有:硝酸铵溶液,氨气,二氧化碳;需要用到的仪器:pH计。已知:镁的化合物不溶于硝酸铵溶液;pH值为11~12时得到较纯净碳酸钙沉淀)。
查看答案和解析>>
科目: 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。如利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
I.CH4(g)=C(s)+2H2(g) ΔH= + 75.0 kJ·mol-1
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH = + 41.0 kJ·mol-1
III.CO(g)+H2(g)=C(s)+H2O(g) ΔH = -131.0 kJ·mol-1
(1)反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH = kJ·mol-1。
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。
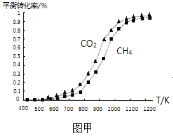
同温度下CO2的平衡转化率 (填“大于”或“小于”)CH4的平衡转化率,其原因是 。
②高温下进行该反应时常会因反应I生成“积碳”(碳单质),造成催化剂中毒,高温下反应I能自发进行的原因是 。
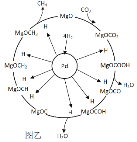
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图乙所示,该反应的化学方程式为 。
(4)CO常用于工业冶炼金属,右图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。下列说法正确的是 。(填序号)
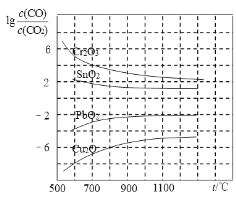
A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应ΔH>0
(5)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2![]() 2CO+O2,则其阳极的电极反应式为 。
2CO+O2,则其阳极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱混合后pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的关系正确的是
A、V(碱)=102V(酸) B、V(碱)=2 V(酸)
C、V(酸)=102V(碱) D、V(酸)=2 V(碱)
查看答案和解析>>
科目: 来源: 题型:
【题目】【物质结构与性质】钛被称为“国防金属”和“生物金属”,是重要的结构材料。
(1)基态钛原子的核外电子排布式是 。
(2)金红石(TiO2)的熔点1825℃,用熔盐法直接电解金红石可获得金属钛,金红石所属的晶体类型是 晶体。
(3)TiCl4能与NH4Cl反应生成配合物(NH4)2[TiCl6]。
①此配合物中,形成配位键时提供孤对电子的有 。(填元素符号)
②与NH4+互为等电子体的一种阴离子为 。(填化学式)
(4)TiO2+与H2O2在稀酸中反应生成橘红色的[TiO(H2O2)]2+离子,可用于钛的定性检验。下列关于H2O2的说法正确的是 。(填序号)
A.空间构型为直线形 |
B.含非极性键的极性分子 |
C.O原子轨道杂化类型为sp3 |
D.化学性质不稳定是因为氢键的键能较小 |
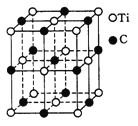
(5)最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,结构模型如图所示,它的分子式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某同学用500 mL容量瓶配制0.10 mol·L-1Na2CO3溶液的步骤:
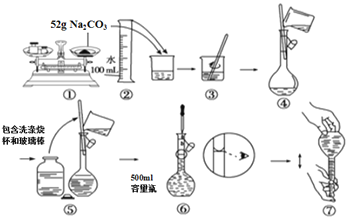
该同学的错误是
A. ①⑤⑥ B. ②④⑦ C. ①⑥ D. ⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.碳酸钠溶液呈碱性,可用于治疗胃酸过多
B.浓度相同的NaNO3溶液和HNO3溶液中NO3-化学性质不同
C.钠的金属性比钾强,工业上用钠制取钾(Na+KCl![]() K↑+NaCl)
K↑+NaCl)
D.既有单质参加,又有单质生成的反应一定是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】36.5gHCl气体溶解在1L水中(水的密度近似为1g/cm3),所得溶液的密度为ρg/ml,质量分数为ω,物质的量浓度为c mol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
A.所得溶液的物质的量浓度为1mol/L
B.所得溶液中含有NA个HCl分子
C.36.5gHCl气体占有的体积为22.4L
D.所得溶液的质量分数:ω=36.5c/(1000ρ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com