
科目: 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Al、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
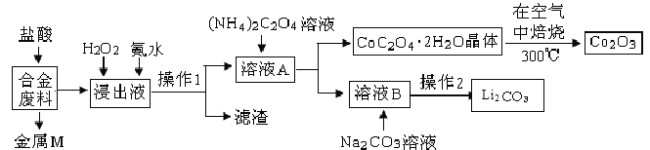
(1) 金属M为 ,操作1所用的玻璃仪器除烧杯外还有 。
(2) 加入H2O2的作用是 (用离子方程式表示),加入氨水的作用是 。
(3) 在空气中焙烧的化学方程式为 。
(4) 已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是 。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/mol·L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(5) 用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1L 0.l mol/L-1 CH3 COOH溶液中加入0.1molCH3COONa固体,溶液中
[c(CH3COO-)·c(H+)]/c(CH3COOH) (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(2)土壤的pH一般在4-9之间。土壤中Na2CO3含量较高,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 ,加入石膏(CaSO4 2H2O)可以使土壤碱性降低,有关反应的化学方程式为
(3)常温下在20ml 0.1mo l·L-1 Na2CO3溶液中逐滴加入0.1mol·L-1 HC1溶液40mL,溶液中含碳元素的各种微粒(CO2)因逸出未画出)物质的量分数随溶液pH变化的情况如图所示。

回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32- (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒为 ,溶液中各种离子的物质的量浓度的大小关系
为 ;
③已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=2×10-4mol·L-1,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH= ;
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2O2与水反应能够产生O2 , 这一反应在呼吸面具、潜水艇及太空飞船中可为人体提供呼吸所用的O2。下面对该反应的说法中正确的是( )
A.这是一个氧化还原反应,Na2O2既是氧化剂,又是还原剂
B.这是一个氧化还原反应,Na2O2是氧化剂,水是还原剂
C.这是一个氧化还原反应,Na2O2是还原剂,水是氧化剂
D.这是一个置换反应,有单质O2产生
查看答案和解析>>
科目: 来源: 题型:
【题目】
①容量瓶 ②蒸馏烧瓶 ③分液漏斗 ④量筒 ⑤烧杯 ⑥托盘天平
(1)加热时必须垫石棉网的有______________
(2)使用时必须检查是否漏水的有______________
(3)标有零刻度的有______________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分子式表示的各组物质一定互为同系物的是( )
A. C2H4和C5H10 B. C2H6和C5H12 C. C2H2和C5H8 D. C2H6O和C5H12O
查看答案和解析>>
科目: 来源: 题型:
【题目】1 mol某链烃最多能和2 mol氯化氢发生加成反应,生成氯代烷1 mol,该氯代烷能和6 mol氯气发生取代反应,生成只含碳元素和氯元素的氯代烃,该烃可能是( )
A.丙烯 B.丙炔 C.1-丁炔 D.1,3-丁二烯
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
A. 体积②>③>①>④ B. 密度②>③>④>①
C. 质量②>③>①>④ D. 氢原子个数①>④>③>②
查看答案和解析>>
科目: 来源: 题型:
【题目】将ag Fe2O3和Al2O3的混合物溶解在过量的200 ml 浓度为0.1 mol/L 的盐酸溶液中,然后向其中加入NaOH溶液,使Fe3+ 、Al3+ 刚好完全沉淀,用去NaOH溶液100ml ,则NaOH溶液的浓度为 ( )
A. 0.1mol/L B. 0.2mol/L C. 0.4mol/L D. 0.8mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com